题目内容
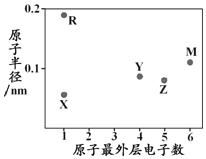
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法中正确的是
A. 简单离子半径:R>M
B. M和Z两种元素可以共存于同一种离子化合物中
C. 工业冶炼R的单质通常用热还原法
D. 氧化物的水化物酸性:Z<M
【答案】B
【解析】
X、Y、Z、M、R为五种短周期元素,由原子半径和最外层电子数之间的关系图可知,X、R最外层只有一个电子,为第IA族元素;Y最外层有4个电子,位于第ⅣA族,Z原子最外层有5个电子,位于第VA族,M最外层有6个电子,位于第VIA族;R原子半径最大,为Na元素,X原子半径最小,为H元素;M原子半径大于Y且最外层电子数大于Y,所以Y是C元素、M为S元素,则Z是N元素,以此解答。
由以上分析可知X为H元素、Y为C元素、Z为N元素、M为S元素、R为Na元素。A.电子层越多,离子半径越大,则简单离子半径:M>R,故A错误;B.Z为N元素、M为S元素,可存在于硫化铵或硫酸铵等离子化合物中,故B正确;C.Na为活泼性较强的金属,应该用电解法冶炼,故C错误;D.如不是最高价氧化物的水化物的酸性,则不能确定酸性强弱,故D错误;故选B。

【题目】(一)常温时,0.1 mol·L-1 NH4Al(SO4)2溶液的pH=3。则溶液中c(NH4+)+c(NH3·H2O)_______c (Al3+) + c[Al(OH)3](填“﹥”、“﹤”或“=”);2c(SO42-)- c(NH4+)-3c(Al3+)=________mol·L-1(填数值)。
(二)金属氢氧化物在酸中的溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下饱和溶液的浓度(mol·L1)如图所示。
(1)pH=3时溶液中铜元素的主要存在形式是________(填化学式)。
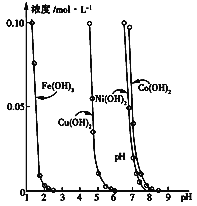
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为______。
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,_____ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_______________________。
(4)要使氢氧化铜沉淀溶解,除加入酸外,还可以加入氨水,生成[Cu(NH3)4]2+,写出发生反应的离子方程式______________________。
(5)已知一些难溶物的溶度积常数如下表。
物质 | FeS | MnS | CuS |
Ksp | 6.3×1018 | 2.5×1013 | 1.3×1036 |
物质[] | PbS | HgS | ZnS |
Ksp | 3.4×1028 | 6.4×1053 | 1.6×1024 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的________(填字母)除去它们。
A.NaOH B.FeS C.Na2S