题目内容
【题目】碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如下图。下列有关该物质的说法正确的是
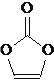
A. 该物质在一定条件下可发生水解反应
B. 分子中含6个σ键
C. 分子中只有极性键
D. 8.6g该物质完全燃烧得到6.72LCO2
【答案】A
【解析】该有机物含有酯基,酯能够发生酸解或碱解,A正确;分子中碳碳双键和碳氧双键中各有1个σ键,碳氧单键全部是σ键(4个),碳氢单键也是σ键(2个),共有8个σ键,B错误;该分子中的碳氧键、碳氢键都是极性键,而碳碳双键属于非极性键,C错误;此选项没有说明温度和压强,以及二氧化碳的状态,所以所得二氧化碳的体积是不确定的,只有在标准状况下,0.3molCO2气体的体积才是6.72L,D错误;正确选项A。

练习册系列答案
相关题目