题目内容
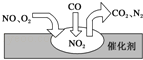
【题目】已知原子序数依次增大的前四周期五种常见元素X、Y、Z、W、R,其相关信息如下:X的原子结构中,最外层电子数是内层电子数的2倍;Z形成的多种同素异形体,其中之一是地球生物的“保护伞”;W的一种单质是黄色粉末,难溶于水,易溶于二硫化碳;R单质在氯气中燃烧会产生棕黄色的烟,该烟溶于少量水中显绿色。
(1)X在元素周期表中的位置:______,该族元素易形成______(填写“离子”或“共价”)化合物。
(2)Y的简单氢化物遇到![]() 可以产生白烟现象,化工上常利用该性质检查氯气,该反应方程式为________。写出该“白烟”的电子式:________。
可以产生白烟现象,化工上常利用该性质检查氯气,该反应方程式为________。写出该“白烟”的电子式:________。
(3)写出Y与Z形成的化合物对环境的影响:__________(写出一条即可)。
(4)Z的一种氢化物可以使酸性高锰酸钾溶液褪色,其原因是__________(用离子方程式表示)。
(5)W的简单氢化物与Z的单质在烧碱溶液中可以形成燃料电池(产物中无沉淀生成),写出负极反应式:____________。
(6)![]() 投入足量的某浓度的硝酸中,所得气体产物为NO和
投入足量的某浓度的硝酸中,所得气体产物为NO和![]() 的混合物,且体积比为1:1,发生反应的化学方程式为:_____________。
的混合物,且体积比为1:1,发生反应的化学方程式为:_____________。
【答案】第二周期ⅣA族 共价 ![]()
![]()
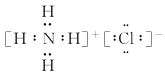 形成酸雨、形成光化学烟雾、造成臭氧空洞等(任写一种即可)
形成酸雨、形成光化学烟雾、造成臭氧空洞等(任写一种即可) ![]()
![]()
![]() =
=![]()
![]()
![]()
【解析】
根据试题提供的信息,可以推理得出X、Y、Z、W、R分别是C、N、O、S、Cu五种元素,据以上几种元素的及其形成化合物的性质进行分析。
根据试题提供的信息,可以推理得出X、Y、Z、W、R分别是C、N、O、S、Cu五种元素。
(1) 碳元素位于元素周期表的第二周期ⅣA族;该族元素一般既不容易失去电子也不容易得到电子,一般易形成共价化合物。
(2) 氨气遇到氯气可以产生白烟现象,是因为生成了氯化铵固体小颗粒,反应原理是![]() ;
;![]() 中含有离子键和共价键,其电子式为
中含有离子键和共价键,其电子式为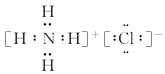 。
。
(3)N与O形成的氮氧化合物对环境的影响主要有形成酸雨、形成光化学烟雾、造成臭氧空洞等。
(4)Z的一种氢化物可以使酸性高锰酸钾溶液褪色,则此氢化物为过氧化氢,其水溶液双氧水具有还原性,和酸性高锰酸钾可以发生氧化还原反应,离子方程式为![]() 。
。
(5)在碱性介质中,![]() 形成的燃料电池会转化为
形成的燃料电池会转化为![]() ,根据题意,可以得出负极反应式为
,根据题意,可以得出负极反应式为![]() =
=![]() 。
。
(6)Cu元素的化合价由+1价升高为+2价,气体产物为NO和![]() 的混合物,且体积比为1:1,得到电子数为4,
的混合物,且体积比为1:1,得到电子数为4,![]() 失去电子数为2,由电子守恒及原子守恒可知,反应为
失去电子数为2,由电子守恒及原子守恒可知,反应为![]() 。
。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案