题目内容
【题目】实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气,所需实验装置如图所示:
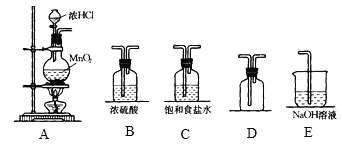
(1)写出装置A中装浓盐酸的仪器名称:______,装置A中发生反应的化学方程式:___________________。
(2)连接上述仪器,仪器的正确连接顺序是___________。
(3)NaOH溶液的作用是_________。
(4)将干燥的Cl2依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是___________,得出的结论是_____________。
【答案】分液漏斗 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O ACBDBE 吸收尾气,防止污染空气 干燥的有色布条不褪色,湿润的有色布条褪色 干燥的氯气不具有漂白性,次氯酸具有漂白性
MnCl2+Cl2↑+2H2O ACBDBE 吸收尾气,防止污染空气 干燥的有色布条不褪色,湿润的有色布条褪色 干燥的氯气不具有漂白性,次氯酸具有漂白性
【解析】
在实验室中,用MnO2与浓盐酸混合加热制取氯气,由于浓盐酸具有挥发性,制取得到的氯气中含有杂质HCl和水蒸气,先通过饱和食盐水除去杂质HCl,然后通过浓硫酸干燥,再根据氯气的密度比空气大,用向上排空气方法收集,最后用NaOH溶液进行尾气处理。
(1)根据图示可知,盛有浓盐酸的仪器名称为分液漏斗;在装置A中MnO2与浓盐酸混合加热制取氯气,发生反应的化学方程式:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)在装置A中制取氯气,通过装置C除去氯气中的杂质HCl,再通过装置B进行干燥,然后由装置D进行气体的收集,为防止最后尾气处理时溶液的水蒸气进入到收集装置,再连接使用装置B,最后用装置E进行尾气处理,所以仪器连接的正确连接顺序是ACBDBE;
(3)NaOH溶液可以与Cl2发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,故NaOH的作用是吸收尾气,防止污染空气;
(4)氯气没有漂白性,而氯气与水反应产生的HClO具有强的氧化性,可以将有色物质氧化变为无色,而具有漂白性,因此将干燥的Cl2依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是干燥的有色布条不褪色,湿润的有色布条褪色,由此得出的结论是:干燥的氯气不具有漂白性,是Cl2与水反应的次氯酸具有漂白性。