题目内容
14.下列反应的离子方程式正确的是( )| A. | 次氯酸钙溶液中通入过量二氧化碳Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 实验室制备氯气 MnO2+4H++4Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl2↑+2H2O | |
| C. | 用氨水吸收少量二氧化硫2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| D. | Cl2通入水中Cl2+H2O?H++Cl-+HClO |
分析 A.二氧化碳过量反应生成碳酸氢钙;
B.电荷不守恒;
C.二氧化硫少量反应生成亚硫酸铵;
D.氯气与水反应生成氯化氢和次氯酸,次氯酸为弱电解质,保留化学式.
解答 解:A.次氯酸钙溶液中通入过量二氧化碳离子方程式:ClO-+H2O+CO2═HCO3-+HClO,故A错误;
B.实验室制备氯气,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故B错误;
C.用氨水吸收少量二氧化硫,离子方程式:2NH3•H2O+SO2═2NH4++SO32-+H2O,故C正确;
D.Cl2通入水中反应生成氯化氢和次氯酸,离子方程式:Cl2+H2O?H++Cl-+HClO,故D正确;
故选:CD.
点评 本题考查离子方程式的正误判断,注意反应物用量对反应的影响,注意原子个数、电荷数守恒,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
4.美国 lawrece liremore 国家实验室(LINL)的V•Lota•C•S•You和H•Cynn成功地在高压下将CO2转化为具有类似SiO2结构的晶体,下列关于CO2的原子晶体的说法正确的是( )
| A. | CO2的原子晶体和分子晶体互为同分异构体 | |
| B. | 在一定的条件下,转化为分子晶体是物理变化 | |
| C. | CO2的原子晶体和分子晶体具有相同的物理性质和化学性质 | |
| D. | 在CO2的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个碳原子结合 |
5.氯水中存在多种分子和离子,它们在不同的反应中表现出不同的性质.下列结论正确的是( )
| A. | 加入有色布条,片刻后有色布条褪色,说明有Cl2存在 | |
| B. | 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2存在 | |
| C. | 先加入盐酸酸化,再加入AgNO3溶液,生成白色沉淀,说明有Cl-存在 | |
| D. | 加入NaOH溶液,氯水的浅黄绿色消失,说明有HClO存在 |
2.用水稀释0.1mol•L-1氨水时,溶液中随水量的增加而减小的是( )
| A. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O}$ | B. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(OH)}$ | C. | n(OH-)和c(H+) | D. | c(H+)和c(OH-)的乘积 |
9.C2H6+Cl2$\stackrel{光照}{→}$C2H5Cl+HCl的反应类型为( )
| A. | 取代反应 | B. | 加成反应 | C. | 酯化反应 | D. | 消去反应 |
19.下列有关说法或操作中,属于正确的有( )
| A. | 用丁达尔效应可区别NaCl溶液和Fe(OH)3胶体 | |
| B. | 用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色的火焰,则原溶液中一定不含有K+ | |
| C. | 用25 mL量筒准确量取4.0 mol/L的盐酸5.62 mL | |
| D. | 配制1.2mol/LNaOH溶液时,若容量瓶中原来有少量蒸馏水,则使实验结果偏低 |
6.在温度t℃下,某Ba(OH)2的稀溶液中?c(H+)=10-amol.L-1,c(OH-)=10-b mol.L-1,已知a+b=12,向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
(1)依据题意判断,t℃大于25℃(填”大于”“小于”或”等于”),该温度下水的离子积KW=1×10-12.
(2)b=4,原Ba(OH)2的稀溶液的物质的量浓度为?5×10-5mol/L?.
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为4,以及其中Na2SO4的物质的量浓度为1×10-4mol/L.
| 序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
(2)b=4,原Ba(OH)2的稀溶液的物质的量浓度为?5×10-5mol/L?.
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为4,以及其中Na2SO4的物质的量浓度为1×10-4mol/L.
3.下列关于苯酚的叙述中,正确的是( )
| A. | 苯酚能与FeCl3溶液反应生成紫色沉淀 | |
| B. | 苯酚呈弱酸性,能使紫色石蕊试液显浅红色 | |
| C. | 向少量苯酚溶液中滴加饱和溴水,可观察到白色沉淀 | |
| D. | 苯酚有强腐蚀性,沾在皮肤上可用水洗涤 |
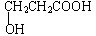 ,该物质易溶于水(填“难”或“易”),原因是能与水分子形成氢键,该物质的熔点明显高于相对分子质量相接近的烃类化合物的熔点,原因是该物质分子间可形成氢键.
,该物质易溶于水(填“难”或“易”),原因是能与水分子形成氢键,该物质的熔点明显高于相对分子质量相接近的烃类化合物的熔点,原因是该物质分子间可形成氢键.