题目内容
3.下列关于苯酚的叙述中,正确的是( )| A. | 苯酚能与FeCl3溶液反应生成紫色沉淀 | |
| B. | 苯酚呈弱酸性,能使紫色石蕊试液显浅红色 | |
| C. | 向少量苯酚溶液中滴加饱和溴水,可观察到白色沉淀 | |
| D. | 苯酚有强腐蚀性,沾在皮肤上可用水洗涤 |
分析 A.苯酚和氯化铁溶液发生显色反应;
B.苯酚具有弱酸性,但不能使石蕊试液变色;
C.苯酚和浓溴水发生取代反应;
D.苯酚具有腐蚀性,常温下在水溶液中溶解度较小,易溶于酒精.
解答 解:A.苯酚和氯化铁溶液发生显色反应而使溶液呈紫色,不生成沉淀,故A错误;
B.苯酚具有弱酸性,酸性很弱,所以不能使石蕊试液变色,故B错误;
C.苯酚和浓溴水发生取代反应生成三溴苯酚白色沉淀,故C正确;
D.苯酚具有腐蚀性,常温下在水溶液中溶解度较小,易溶于酒精,所以沾在皮肤上可用酒精洗涤,故D错误;
故选C.
点评 本题考查苯酚性质,明确官能团及性质关系即可解答,利用酚羟基的显色反应、和溴水反应生成沉淀可以鉴定酚羟基的存在,注意酚发生取代反应时苯环上氢原子的取代位置,为易错点.

练习册系列答案
相关题目
13.下列有机物的命名正确的是( )
| A. | 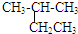 2-乙基丙烷 2-乙基丙烷 | B. | CH3CH2CHBrCH3 2-溴丁烷 | ||
| C. |  间二甲苯 间二甲苯 | D. | 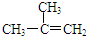 2-甲基-2-丙烯 2-甲基-2-丙烯 |
14.下列反应的离子方程式正确的是( )
| A. | 次氯酸钙溶液中通入过量二氧化碳Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 实验室制备氯气 MnO2+4H++4Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl2↑+2H2O | |
| C. | 用氨水吸收少量二氧化硫2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| D. | Cl2通入水中Cl2+H2O?H++Cl-+HClO |
11.已知X、Y是核电荷数不大于18的元素.X原子的最外层电子数为a,次外层电子数为a+2;Y原子的最外层电子数为b-5,次外层电子数为b.判断X、Y元素形成的化合物组成是( )
| A. | XY2 | B. | Y2X3 | C. | Y4X | D. | YX3 |
18.下列说法正确的是( )
| A. | 构成原电池正极和负极的材料必须是金属 | |
| B. | 在原电池中,电子流出的一极是负极,该电极被还原 | |
| C. | 实验室欲快速制取氢气,可利用粗锌与稀H2SO4反应 | |
| D. | 原电池可以把物质内部的能量全部转化为电能 |
12.下列各项中表达正确的是( )
| A. | H、D、T表示同一种核素 | |
| B. | F-离子结构示意图: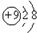 | |
| C. | 用电子式表示HCl形成过程:H${\;}_{\;}^{•}$+${\;}_{\;}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$→H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| D. | 次氯酸电子式:H${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$ |
 ;
; ;
;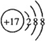 ;
; .
. $\stackrel{KMnO_{4}}{→}$
$\stackrel{KMnO_{4}}{→}$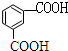
 ;
;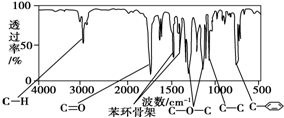 化合物A经李比希法测得其 中含C 72.0%、H 6.67%,其余含有氧;质谱法分析得知A的相对分子质量为150.现代仪器分析有机化合物的分子结构有以下两种方法.
化合物A经李比希法测得其 中含C 72.0%、H 6.67%,其余含有氧;质谱法分析得知A的相对分子质量为150.现代仪器分析有机化合物的分子结构有以下两种方法.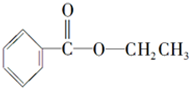 、
、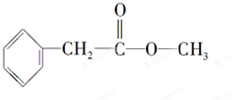 ;
; .
.