题目内容
【题目】已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如下表:
H2CO3 | H2SO3 | HClO |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
K2=5.61×10-11 | K2=1.02×10-7 |
下列说法正确的是
A. 相同条件下,同浓度的 H2SO3溶液和 H2CO3溶液的酸性, 后者更强
B. Na2CO3溶液中通入少量SO2: 2CO3 2- + SO2+ H2O = 2HCO3 - + SO3 2-
C. NaClO 溶液中通入少量CO2:2ClO- + CO2 + H2O = 2HClO + CO3 2-
D. 向氯水中分别加入等浓度的 NaHCO3 和 NaHSO3溶液,均可提高氯水中 HClO 的浓度
【答案】B
【解析】A、弱电解质的电离平衡常数越大,则电离程度越大,说明弱酸的酸性越强,或者弱碱的碱性越强,H2SO3的K1=1.54×10-2,而H2CO3的K1=4.30×10-7,所以同浓度时H2SO3的酸性强于H2CO3的,故A错误;B、由于H2SO3的K2小于H2CO3的K1,但大于其K2,所以Na2CO3溶液中通入少量SO2,考虑Na2CO3与酸的分步反应,所以反应的离子方程式为2CO32- + SO2 + H2O =2HCO3- + SO32-,当SO2足量时,生成CO2和HSO3-,所以B正确;C、已知HClO的K=2.95×10-8大于H2CO3的K2,但小于其K1,所以NaClO溶液中通入少量CO2,反应的离子方程式为ClO- + CO2 + H2O = HClO + HCO3-,故C错误;D、由于HClO的K=2.95×10-8小于H2CO3的K1,但大于其K2,因此HClO不能与NaHCO3反应,但HCl是强酸,能与NaHCO3反应,使c(HCl)减小,促进化学平衡Cl2+H2O![]() HCl+HClO正向移动,从而提高HClO的浓度;尽管HClO的K=2.95×10-8小于H2SO3的K1=1.54×10-2,也小于H2SO3的K2=1.02×10-7,只是说明NaHSO3不能与HClO发生复分解反应,但HClO具有氧化性,NaHSO3具有还原性,二者能够发生氧化还原反应,所以加入NaHSO3溶液不能提高HClO的浓度,故D错误。本题正确答案为B。
HCl+HClO正向移动,从而提高HClO的浓度;尽管HClO的K=2.95×10-8小于H2SO3的K1=1.54×10-2,也小于H2SO3的K2=1.02×10-7,只是说明NaHSO3不能与HClO发生复分解反应,但HClO具有氧化性,NaHSO3具有还原性,二者能够发生氧化还原反应,所以加入NaHSO3溶液不能提高HClO的浓度,故D错误。本题正确答案为B。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案【题目】下列物质与水反应生成强碱的是( )
A. NH3 B. Na2O C. CO2 D. NO2
【答案】B
【解析】
A. NH3溶于水生成一水合氨,属于弱碱,A错误;B. Na2O溶于水生成氢氧化钠,是强碱,B正确;C. CO2溶于水生成碳酸,属于弱酸,C错误;D. NO2溶于水生成硝酸和NO,硝酸是强酸,D错误,答案选B。
【题型】单选题
【结束】
19
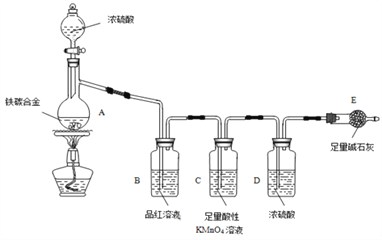
【题目】利用下列装置可以完成的实验组合是

选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
C | Zn 稀硫酸 | 浓硫酸 | H2 |
D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
A. AB. BC. CD. D