题目内容
【题目】甲醇(CH3OH )是一种用途广泛的基础有机原料和优质燃料。
(1)甲醇可以在铜作催化剂的条件下直接氧化成甲醛(HCHO)
①基态Cu原子的价层电子的轨道表达式为_____,其核外电子共占据_____个能级。
②甲醇和甲醛中碳原子的杂化方式分别为_____,其组成元素的电负性由小到大的顺序为________.
(2)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,佛点57.1℃)
①乙酸甲酯分子中心键和节键的个数之比为_________;
②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,工业上用蒸馏的方法分离二者时常先加适量水,理由为______________。
(3)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成T一碳,T-碳的晶体结构可以看成金刚石晶体中每个碳原子被- 一个由四个碳原子组成的正四面体结构单元取代,如图所示。
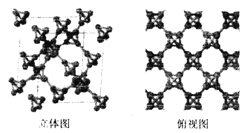
①T-碳与金刚石互称为_________;一个T-碳晶胞中含有______个碳原子。
②T-碳的密度非常小,约为金刚石的一半。试计算T-碳晶胞的边长和金刚石品胞的边长之比为________。
【答案】 ![]() 7 sp3、sp2 H、C、O 10:1 乙酸甲酯不易与水形成氢键,而甲醇易与水形成氢键使甲醇沸点升高,使得乙酸甲酯容易从混合物中蒸出 同素异形体 32 2:1
7 sp3、sp2 H、C、O 10:1 乙酸甲酯不易与水形成氢键,而甲醇易与水形成氢键使甲醇沸点升高,使得乙酸甲酯容易从混合物中蒸出 同素异形体 32 2:1
【解析】(1)①Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1,,价层电子的轨道表达式为![]() ,其核外电子共占据7个能级;②甲醇中碳原子的杂化方式为 sp3,而甲醛中碳原子的杂化方式为 sp2,元素非金属性越强电负性越大,则其组成元素C、H、O的电负性由小到大的顺序为H、C、O;(2)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,佛点57.1℃)
,其核外电子共占据7个能级;②甲醇中碳原子的杂化方式为 sp3,而甲醛中碳原子的杂化方式为 sp2,元素非金属性越强电负性越大,则其组成元素C、H、O的电负性由小到大的顺序为H、C、O;(2)在一定条件下,甲醇(沸点64.7℃)可转化为乙酸甲酯(CH3COOCH3,佛点57.1℃)
①乙酸甲酯分子中除了碳氧双键中含一个![]() 键和一个
键和一个![]() 键外,另有9个
键外,另有9个![]() 键,故
键,故![]() 键和
键和![]() 键的个数之比为10:1;②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,乙酸甲酯不易与水形成氢键,而甲醇易与水形成氢键使甲醇沸点升高,使得乙酸甲酯容易从混合物中蒸出,故工业上用蒸馏的方法分离二者时常先加适量水;(3)①T-碳与金刚石是由碳形成的不同单质,互称为同素异形体;金刚石的晶胞是18个碳原子(顶点8个,面心上下左右前后6个,体内两层对角线各2个共4个),运用切割法, 一个晶胞中的应是
键的个数之比为10:1;②甲醇与乙酸甲酯的混合物因沸点接近而不易分离,乙酸甲酯不易与水形成氢键,而甲醇易与水形成氢键使甲醇沸点升高,使得乙酸甲酯容易从混合物中蒸出,故工业上用蒸馏的方法分离二者时常先加适量水;(3)①T-碳与金刚石是由碳形成的不同单质,互称为同素异形体;金刚石的晶胞是18个碳原子(顶点8个,面心上下左右前后6个,体内两层对角线各2个共4个),运用切割法, 一个晶胞中的应是![]() 个碳原子;T-碳的晶体结构可以看成金刚石晶体中每个碳原子被- 一个由四个碳原子组成的正四面体结构单元取代,故含有碳个数为32个;②T-碳的密度非常小,约为金刚石的一半,而根据构成原子的数目,质量为金刚石的4倍,根据V=
个碳原子;T-碳的晶体结构可以看成金刚石晶体中每个碳原子被- 一个由四个碳原子组成的正四面体结构单元取代,故含有碳个数为32个;②T-碳的密度非常小,约为金刚石的一半,而根据构成原子的数目,质量为金刚石的4倍,根据V=![]() ,T-碳晶胞的体积应该是金刚石的8倍,而边长=
,T-碳晶胞的体积应该是金刚石的8倍,而边长=![]() ,则边长为金刚石的2倍,即T-碳晶胞的边长和金刚石品胞的边长之比为2:1。
,则边长为金刚石的2倍,即T-碳晶胞的边长和金刚石品胞的边长之比为2:1。

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案【题目】已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如下表:
H2CO3 | H2SO3 | HClO |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
K2=5.61×10-11 | K2=1.02×10-7 |
下列说法正确的是
A. 相同条件下,同浓度的 H2SO3溶液和 H2CO3溶液的酸性, 后者更强
B. Na2CO3溶液中通入少量SO2: 2CO3 2- + SO2+ H2O = 2HCO3 - + SO3 2-
C. NaClO 溶液中通入少量CO2:2ClO- + CO2 + H2O = 2HClO + CO3 2-
D. 向氯水中分别加入等浓度的 NaHCO3 和 NaHSO3溶液,均可提高氯水中 HClO 的浓度