题目内容
有四种元素xA、yB、zC、mD,x、y、z、m为质子数.己知:
①C、D、B在同一周期,其中B原子的L层电子数比K层和M层电子数之和少一个;
②D的+1价阳离子的电子层结构与Ne原子相同;
③A原子的质子数与中子数相等,且A的原子质量数与D的中子数相等,而C的质子数比中子数少一个;x+y+z+m=48.试回答:
(1)A为______.在周期表中位置______;D的离子结构示意图______.
(2)写出A、B、C、D的最高价氧化物的分子式:______.
(3)写出C、D最高价氧化物水化物反应的化学方程式______,A的最高价氧化物与D的最高价氧化物的水化物反应的化学方程式______.
(4)写出A的氧化物的结构式______,分子空间构型为______.
①C、D、B在同一周期,其中B原子的L层电子数比K层和M层电子数之和少一个;
②D的+1价阳离子的电子层结构与Ne原子相同;
③A原子的质子数与中子数相等,且A的原子质量数与D的中子数相等,而C的质子数比中子数少一个;x+y+z+m=48.试回答:
(1)A为______.在周期表中位置______;D的离子结构示意图______.
(2)写出A、B、C、D的最高价氧化物的分子式:______.
(3)写出C、D最高价氧化物水化物反应的化学方程式______,A的最高价氧化物与D的最高价氧化物的水化物反应的化学方程式______.
(4)写出A的氧化物的结构式______,分子空间构型为______.
有四种元素xA、yB、zC、mD,x、y、z、m为质子数.D的+1价阳离子的电子层结构与Ne原子相同,则D为Na元素;C、D、B在同一周期,处于第二周期,B原子的L层电子数比K层和M层电子数之和少一个,则其M层电子数为8+1-2=7,则B为Cl元素;A原子的质子数与中子数相等,且A的原子质量数与D的中子数相等,则A原子质子数为
=6,故A为碳元素;x+y+z+m=48,则z=48-6-11-17=14,故C为Si元素,
(1)A为碳元素,在周期表中位置为:第二周期ⅣA族;D为Na元素,其离子结构示意图为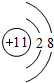 ,故答案为:碳;第二周期ⅣA族;
,故答案为:碳;第二周期ⅣA族;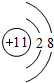 ;
;
(2)C、Cl、Si、Na的最高价氧化物的分子式分别为:CO2,Cl2O7,SiO2,Na2O,故答案为:CO2,Cl2O7,SiO2,Na2O;
(3)Si、Na最高价氧化物水化物为H2SiO3、NaOH,反应的化学方程式为H2SiO3+2NaOH
Na2SiO3+2H2O,A的最高价氧化物CO2,与NaOH反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O,
故答案为:H2SiO3+2NaOH=Na2SiO3+2H2O;CO2+2NaOH=Na2CO3+H2O;
(4)A的氧化物为CO2,结构式为O=C=O,分子空间构型为直线型,故答案为:O=C=O;直线型.
| 12 |
| 2 |
(1)A为碳元素,在周期表中位置为:第二周期ⅣA族;D为Na元素,其离子结构示意图为
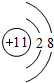 ,故答案为:碳;第二周期ⅣA族;
,故答案为:碳;第二周期ⅣA族;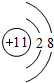 ;
;(2)C、Cl、Si、Na的最高价氧化物的分子式分别为:CO2,Cl2O7,SiO2,Na2O,故答案为:CO2,Cl2O7,SiO2,Na2O;
(3)Si、Na最高价氧化物水化物为H2SiO3、NaOH,反应的化学方程式为H2SiO3+2NaOH
| ||
故答案为:H2SiO3+2NaOH=Na2SiO3+2H2O;CO2+2NaOH=Na2CO3+H2O;
(4)A的氧化物为CO2,结构式为O=C=O,分子空间构型为直线型,故答案为:O=C=O;直线型.

练习册系列答案
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目