题目内容
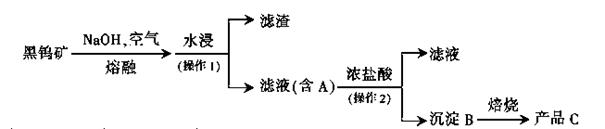
锶(Sr)为第五周期第II A族元素。高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,用工业碳酸锶粉末(含少量钡、铁的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。
已知:SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。请回答:
(1)操作①加快反应速率的措施有 (任写一种方法)。碳酸锶与盐酸反应的离子方程式为 。
(2)加入少量30% H2O2溶液的发生反应的离子方程式为 。
(3)步骤③中调节溶液pH至8—10,宜选用的试剂为_______(填序号):
A.氨水 B.氢氧化钠 C. 氢氧化锶粉末 D.碳酸钠晶体
所得滤渣的主要成分是Fe(OH)3和 (填化学式)。
(4)工业上用热风吹干六水氯化锶,选择的适宜温度范围是 。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(5)若滤液中Ba2+ 浓度为1×10-5mol/L,依下表数据推算出滤液中Sr2+物质的量浓度不大于 mol/L。
| | SrSO4 | BaSO4 | Sr(OH)2 |
| Ksp | 3.3×10—7 | 1.1×10—10 | 3.2×10—4 |
(16分)
(1)(共5分)升高温度、或增大盐酸浓度、或充分搅拌等(合理均可,2分)
SrCO3+2H+=Sr2++CO2↑+H2O (3分)
(2)(共3分)2Fe2++H2O2+2H+=2Fe3++2H2O
(3)(共4分)C(2分) BaSO4(2分)
(4)(共2分) A
(5)(共2分)0.03(或3×10-2)
[计算过程:c(SO42-)=1.1×10-10÷10-5 mol?L-1=1.1×10-5 mol?L-1,c(Sr2+)=3.3×10-7÷1.1×10-5 mol?L-1=3×10-2 mol?L-1]
解析试题分析:(1)根据影响化学反应速率的因素,升高温度、或增大盐酸浓度、或充分搅拌等都能加快反应速率;盐酸的酸性比碳酸强,因此碳酸锶与盐酸能发生复分解反应,同主族元素具有相似性,镁、钙、锶、钡都是第IIA族,碳酸镁微溶、碳酸钙难溶、碳酸钡难溶,由此推断碳酸锶难溶于水,应保留化学式,则该反应为SrCO3+2H+=Sr2++CO2↑+H2O;
(2)铁的化合物溶于盐酸时可能生成亚铁离子和铁离子,双氧水具有强氧化性,是绿色氧化剂,可以将亚铁离子氧化为铁离子,即2Fe2++H2O2+2H+=2Fe3++H2O,便于除铁;
(3)氨水与氢离子容易结合成铵根离子,虽然能消耗氢离子,升高溶液的pH,但是引入的铵根离子是新的杂质,故A选项错误;氢氧化钠也能消耗氢离子,达到调节溶液pH的目的,但是引入的钠离子是新的杂质,故B选项错误;氢氧化锶能消耗氢离子,将溶液pH调至8~10,且引入的锶离子是目标产物需要的离子,故C选项正确;碳酸钠能消耗氢离子,但是会引入钠离子,故D选项错误;由于钡的化合物溶于盐酸产生钡离子,加入过量硫酸时,硫酸根离子与钡离子结合生成硫酸钡沉淀,则滤渣的主要成分是氢氧化铁和硫酸钡;
(4)由于SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水,为了减少目标产物的损失,不能使温度达到61℃或61℃以上,故只有A选项正确;
(5)由于BaSO4(s) Ba2++SO42—,Ksp(BaSO4)=c(Ba2+)?c(SO42—),则滤液中c(SO42—)= 1.1×10—10÷1×10-5 mol/L =1.1×10—5mol/L,由于SrSO4(s)
Ba2++SO42—,Ksp(BaSO4)=c(Ba2+)?c(SO42—),则滤液中c(SO42—)= 1.1×10—10÷1×10-5 mol/L =1.1×10—5mol/L,由于SrSO4(s) Ba2++SO42—,为了防止锶离子沉淀,则Qc(SrSO4)=c(Sr2+)?c(SO42—)≤Ksp(SrSO4),则滤液中c(Sr2+)≤3.3×10—7÷1.1×10-5 mol/L =3.0×10—2mol/L。
Ba2++SO42—,为了防止锶离子沉淀,则Qc(SrSO4)=c(Sr2+)?c(SO42—)≤Ksp(SrSO4),则滤液中c(Sr2+)≤3.3×10—7÷1.1×10-5 mol/L =3.0×10—2mol/L。
考点:考查物质制备化学工艺流程,涉及加快酸浸反应速率的措施、盐酸与碳酸锶反应的离子方程式、加入过氧化氢时反应的离子方程式、选择合理的试剂调节溶液pH除杂、滤渣的成分、选择合适的烘干温度、硫酸钡和硫酸锶溶度积的计算等。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):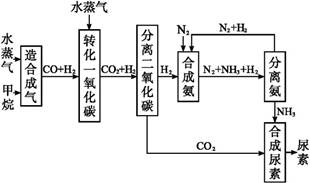
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是 。
(2)上述流程中,工业上分离H2、CO2合理的方法是 。
| A.混合气先通入氢氧化钠溶液,再在溶液中加入盐酸 |
| B.混合气加压冷却,使CO2液化 |
| C.混合气用氨水洗涤 |
| D.混合气先通入石灰浆中,然后高温煅烧固体 |
(4)合理地利用资源不仅可以提高经济效益,也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(己知Cd的金属活动性介于Zn和Fe之间)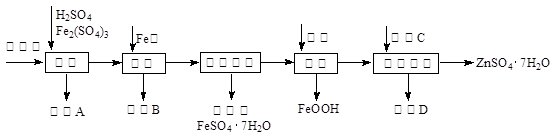
(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为 。
(2)浸取过程中Fe2(SO4)3的作用是 ,浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为 。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为 。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是 。
(4)置换法除重金属离子是Cd2+,所用物质C为 。
(5)硫酸锌的溶解度与温度之间的关系如下表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
从除重金属后的硫酸锌溶液中获得硫酸锌晶体的实验操作为 、 、过滤、干燥。
化学工业是国民经济的支柱产业,下列生产过程中不涉及化学变化的是
| A.氮肥厂用氢气和氮气合成氨 | B.钢铁厂用热还原法冶炼铁 |
| C.工业上常用接触法生产硫酸 | D.炼油厂用分馏法生产汽油 |
在硫酸的工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是( )
| A.硫铁矿煅烧前将要矿粒粉碎,因为大块的硫铁矿不能燃烧 |
| B.从沸腾炉出来的炉气需净化,因为炉气中SO2会与杂质反应 |
| C.SO2氧化为SO3时需使用催化剂,这样可以提高SO2的转化率 |
| D.SO3用质量分数为98%的浓H2SO4吸收,目的是防止形成酸雾,以便使SO3吸收完全 |
下列工业生产中,各物质的物质的量间的关系式不正确的是( )
| A.制漂白粉:2Cl2~Ca(ClO)2 |
| B.制H2SO4:FeS2~2H2SO4 |
| C.合成氨:C~H2~2/3NH3 |
| D.制HNO3:NH3~HNO3 |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )。
2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )。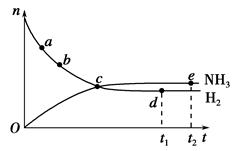
| A.点a的正反应速率比点b的小 |
| B.点c处反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值大 |


 Li7Ti5O12+3FePO4
Li7Ti5O12+3FePO4