题目内容
化学工业是国民经济的支柱产业,下列生产过程中不涉及化学变化的是
| A.氮肥厂用氢气和氮气合成氨 | B.钢铁厂用热还原法冶炼铁 |
| C.工业上常用接触法生产硫酸 | D.炼油厂用分馏法生产汽油 |
D
解析试题分析:A、N2和H2合成NH3发生了化学变化,错误;B、钢铁厂炼铁的原理是利用还原剂将铁从其氧化物中还原出来,发生的是化学变化,错误;C、接触法制硫酸主要有三个步骤:S→SO2→SO3→H2SO4,三个步骤均发生化学反应,错误;D、炼油厂用分馏法生产汽油是利用沸点的不同进行混合物的分离操作,属物理变化,正确。
考点:考查工业生产原理、物理变化和化学变化的区别。

锶(Sr)为第五周期第II A族元素。高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,用工业碳酸锶粉末(含少量钡、铁的化合物等杂质)制备高纯六水氯化锶晶体的过程如下图所示。
已知:SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。请回答:
(1)操作①加快反应速率的措施有 (任写一种方法)。碳酸锶与盐酸反应的离子方程式为 。
(2)加入少量30% H2O2溶液的发生反应的离子方程式为 。
(3)步骤③中调节溶液pH至8—10,宜选用的试剂为_______(填序号):
A.氨水 B.氢氧化钠 C. 氢氧化锶粉末 D.碳酸钠晶体
所得滤渣的主要成分是Fe(OH)3和 (填化学式)。
(4)工业上用热风吹干六水氯化锶,选择的适宜温度范围是 。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(5)若滤液中Ba2+ 浓度为1×10-5mol/L,依下表数据推算出滤液中Sr2+物质的量浓度不大于 mol/L。
| | SrSO4 | BaSO4 | Sr(OH)2 |
| Ksp | 3.3×10—7 | 1.1×10—10 | 3.2×10—4 |
下列说法中,不正确的是
| A.现代科学技术的发展和环境问题的解决离不开化学科学 |
| B.门捷列夫提出的元素周期律为发现新元素、合成新材料提供了新思路 |
| C.绿色化学最显著的特征是在生产化工产品过程中必须利用绿色植物为原料 |
| D.植物的光合作用是地球上规模最大的化学反应,在生物体内把光能转变为化学能 |
下列物质的制备,符合工业生产实际的是
| A.电解饱和氯化钠溶液制备金属钠 |
| B.将氨气与二氧化碳先后通入饱和食盐水中,生成碳酸氢钠沉淀,再生成纯碱 |
| C.将氢气和氯气混合后点燃,产物用浓盐酸吸收制备盐酸 |
| D.将SO2和O2的混合气加压后,通过接触室制备SO3 |
水是生命之源,也是重要的环境要素之一。
(1)观察下图(Ⅰ),若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是__________。
| A.100 mL烧杯 | B.50 mL烧杯 | C.100 mL量筒 | D.50 mL量筒 |
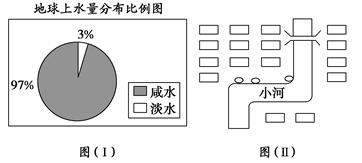
(2)图(Ⅱ)是某居民小区中垃圾收集点(小圈)的布局,它在选址上存在的问题有________;垃圾收集点选址应考虑的因素包括__________________________
(3)有人设想在住宅小区附近建立小型生活垃圾焚烧厂,其流程如图(Ⅲ)。请将图(Ⅲ)中①②③所要表达的内容填在下面的横线上。

图(Ⅲ)
①______________________________;
②________________________________;
③_________________________________。
科学家及一些实业家的贡献对科学的发展起着积极地推动作用。下列对有关科学家及其发明创造的叙述,错误的是
| A.拉瓦锡证明了化学反应中的质量守恒,建立了燃烧的新理论 |
| B.舍勒发现了氯气,凯库勒提出了苯的结构式 |
| C.侯德榜发明了“候氏制碱”法,吴蕴初开创了中国的氯碱工业 |
| D.道尔顿、汤姆孙、卢瑟福和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献 |
下列对硫酸生产中化学反应原理的分析正确的是 ( )。
| A.硫酸生产中涉及的三个化学反应因原料的不同可能全部是非氧化还原反应 |
| B.硫酸生产中涉及的三个化学反应都是放热反应 |
| C.硫酸生产中涉及的三个化学反应都需要使用催化剂 |
| D.硫酸生产中涉及的三个化学反应都需要在较高温度条件下进行 |
下列化学工业有关设备、原料、反应条件配套的是 ( )
| A.联合制碱法制纯碱:吸氨塔、碳酸塔、食盐、二氧化碳、氨、30 ℃~35 ℃的氨化饱和食盐水吸收CO2 |
| B.接触法制硫酸:氧化炉、硫铁矿、V2O5、4000~5000 ℃ |
| C.合成氨:沸腾炉、焦炭、铁触媒、500 ℃ |
| D.氨氧化法制硝酸:合成塔、空气、铂铑合金、8000 ℃ |

 2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)