题目内容
【题目】NH3是一种重要的化工原料,也是造成水体富营养化及氮氧化物污染的重要因素之一。
(1)N2和H2以物质的量之比为1∶3在不同温度和压强下发生反应:N2+3H2![]() 2NH3,测得平衡体系中NH3的物质的量分数如图1。
2NH3,测得平衡体系中NH3的物质的量分数如图1。
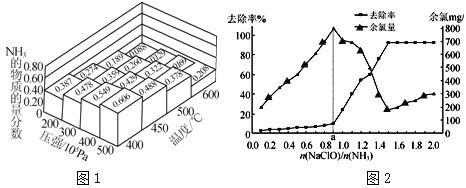
①为提高原料气的转化率,工业上采取的合理措施有 (填字母)。
a. 采用常温条件
b. 使用适当的催化剂
c. 将原料气加压
d. 将氨液化并不断移出
②图1中所示的平衡体系中NH3的物质的量分数为0.549和0.488时,该反应的平衡常数分别为K1、K2,则K1 K2。(填“>”“<”或“=”)
(2)氨氮是造成水体富营养化的重要因素之一,用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,涉及的相关反应如下:
反应①:NH3+HClO===NH2Cl+H2O
反应②:NH2Cl+HClO===NHCl2+H2O
反应③:2NHCl2+H2O===N2+HClO+3HCl
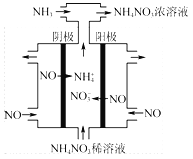
已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件一定的情况下,改变![]() (即NaClO溶液的投入量),溶液中次氯酸钠对氨氮去除率及余氯量 (溶液中+1价氯元素的含量)的影响如图2所示。
(即NaClO溶液的投入量),溶液中次氯酸钠对氨氮去除率及余氯量 (溶液中+1价氯元素的含量)的影响如图2所示。
①反应中氨氮去除效果最佳的n(NaClO)/n(NH3)值约为 。
②a点之前氨氮去除率较低的原因为 。
(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图3。
①电解过程(虚线内)发生反应的离子方程式为 。
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为 。
【答案】(1)①cd
②>
(2)①1.5
② NaClO用量较少,水解生成的少量HClO与NH3主要发生反应①,生成较稳定的NH2Cl。
(3)①8NO + 7H2O![]() 2H+ + 3NH4+ + 5NO3—
2H+ + 3NH4+ + 5NO3—
②1:4
【解析】
试题分析:(1)①a.采用常温条件,化学反应速率慢,故a错误;b.采用适当的催化剂,加快合成氨的速率,但不能改变转化率,故b错误;c.将原料气加压,加快了合成氨的速率,平衡正向移动,故c正确;d.将氨液化,不断移去液氨,平衡正向移动,故d正确。
故答案为: cd;
②图1中所示的平衡体系中NH3的物质的量分数为0.549的温度是400℃,0.478时的温度是450℃,该反应为放热反应,温度升高平衡向逆反应方向移动,K减小。所以,K1>K2。
故答案为:>;
(2)用次氯酸钠水解生成的次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,改变![]() (即NaClO溶液的投入液),溶液中次氯酸钠去除氨氮效果与余氯图象变化中,次氯酸少氨气多,a点前发生的反应是NH3(aq)+HClO(aq)═NH2Cl(aq)+H2O(l),生成较稳定的NH2Cl;反应中氨氮去除效果最佳的从图象分析可知为去除率较高同时余氯量最少,图象中符合的比值为1.5。
(即NaClO溶液的投入液),溶液中次氯酸钠去除氨氮效果与余氯图象变化中,次氯酸少氨气多,a点前发生的反应是NH3(aq)+HClO(aq)═NH2Cl(aq)+H2O(l),生成较稳定的NH2Cl;反应中氨氮去除效果最佳的从图象分析可知为去除率较高同时余氯量最少,图象中符合的比值为1.5。
故答案为:1.5; NaClO用量较少,水解生成的少量HClO与NH3主要发生反应①,生成较稳定的NH2Cl。
(3)①工业上电解NO制备 NH4NO3,由装置图可知阳极发生氧化反应,NO被氧化生成NO3-,阴极发生还原反应,NO被还原生成NH4+,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,总反应方程式为:8NO+7H2O![]() 3NH4NO3+2HNO3。
3NH4NO3+2HNO3。
故答案为:8NO+7H2O![]() 3NH4NO3+2HNO3;
3NH4NO3+2HNO3;
②生成的硝酸和反应的NO的物质的量之比等于2:8=1:4,通入的NH3的物质的量至少应与生成的硝酸的物质的量相等,因此通入的NH3与实际参加反应的NO的物质的量之比至少为1:4。
故答案为:1:4。

 阅读快车系列答案
阅读快车系列答案