题目内容
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nsnnpn |
B | 基态原子中的未成对电子数是同周期中最多的 |
C | 原子最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
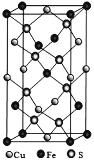
(1)E元素在周期表中的位置是_________________________。
(2)写出D元素基态原子的简化电子排布式:__________。
(3)这5种元素中电负性最大的元素是__________(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为_______________________(填元素符号)。
(4)B、C、D的简单离子的半径由大到小的顺序为____________(用离子符号表示)。
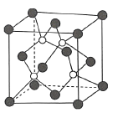
(5)写出C的核外有18个电子的氢化物的电子式:_____________________。
【答案】第四周期Ⅷ族 [Ne]3s23p1 O N>O>C N3->O2->Al3+ ![]()
【解析】
A元素基态原子的价电子排布式为nsnnpn,由于s能级最多填充2个电子,则n=2,价层电子排布为2s22p2,所以A是碳元素;D元素简单离子是第三周期元素中离子半径最小的,则D是Al元素;C元素最外层电子数是电子层数的3倍,原子序数小于Al,则C是O元素,B元素基态原子中的未成对电子数是同周期中最多的,则B是N元素;E元素价电子层中的未成对电子数为4,则E的价层电子排布是3d64s2,即为铁元素,结合选项分析解答。
(1)E是铁元素,铁是26号元素,位于元素周期表第四周期Ⅷ族;
(2)D是Al元素的原子序数是13,其基态原子的简化电子排布式为[Ne]3s23p1;
(3)非金属性越强,电负性越大,则这5种元素中电负性最大的元素是O;非金属性越强,第一电离能越大,但由于氮元素的2p轨道电子处于半充满状态,稳定性强,则A、B、C三种元素的第一电离能由大到小的顺序为N>O>C;
(4)核外电子排布相同的离子,其离子半径随原子序数的增大而减小,则B、C、D的简单离子的半径由大到小的顺序为N3->O2->Al3+;
(5)氧元素的核外有18个电子的氢化物是双氧水,属于共价化合物,电子式为![]() 。
。

【题目】甲醇是重要的化工原料,在有机合成中具有广泛应用。
(1)用甲醇制取甲胺的反应为:CH3OH(g)+NH3(g)CH3NH2(g)+H2O(g)△H
已知该反应中相关化学键的键能数据如下:
共价键 | C―O | H―O | N―H | C―N |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 |
则该反应的△H=______kJ·mol-1
(2)一定条件下,将2mol CO和6mol H2通入2L密闭容器中发生如下反应:
主反应:CO(g)+2H2(g)CH3OH(g)△H<0 Ⅰ
副反应:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0 Ⅱ
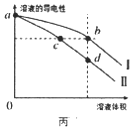
反应到t min时,达到平衡状态。平衡时CH3OH的体积分数φ(CH3OH)随温度、压强的变化如图所示:
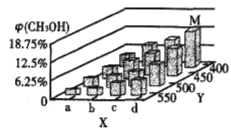
①图中a___b(填“大于”或“小于”)。图中Y轴表示温度,其理由是_________;
②若反应II的平衡常数K值变小,则下列说法中正确的是___________(填序号)。
A.平衡均向正反应方向移动 B.平衡移动的原因是升高了温度
C.达到新平衡后,φ(CH3OH)减小 D.容器中φ(CH3OCH3)增大
③平衡时,M点CH3OH的体积分数为12.5%,c(CH3OCH3)=0.1mol·L-1,则此时CO的转化率为_____;用H2表示I的反应速率为_____mol·L-1·min-1。
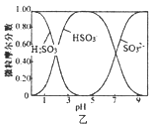
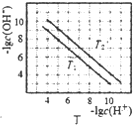
(3)用NaOH溶液做CO2碳捕捉剂,在降低碳排放的同时也获得了重要的化工产品Na2CO3。常温下,若某次捕捉后得到pH=11的溶液,则溶液中c(![]() )∶c(
)∶c(![]() )=___________[已知H2CO3的电离平衡常数为:K1=4.4×107、K2=5×1011],溶液中c(Na+)_______ c(
)=___________[已知H2CO3的电离平衡常数为:K1=4.4×107、K2=5×1011],溶液中c(Na+)_______ c(![]() )+2c(
)+2c(![]() )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。