题目内容
19.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图所示.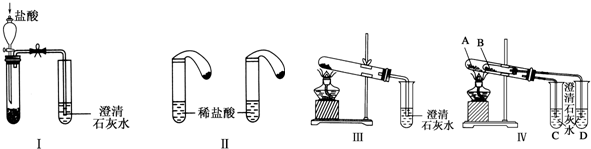
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的是Ⅱ(填装置序号).
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)与实验Ⅲ相比,实验Ⅳ的优点是D(填选项序号).
A、Ⅳ比Ⅲ复杂
B、Ⅳ比Ⅲ安全
C、Ⅳ比Ⅲ操作简便
D、Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(4)Ⅲ中加热碳酸氢钠时,澄清石灰水会变浑,石灰水变浑反应的离子方程式CO2+Ca2++2OH-=CaCO3↓+H2O.
(5)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入物固体最好是NaHCO3(填化学式).
分析 (1)I中均与盐酸反应生成二氧化碳,石灰水均变浑浊;而Ⅱ中均与盐酸反应生成气体,但气球变大的快慢不同;
(2)图Ⅲ、Ⅳ均为加热法鉴别,碳酸氢钠加热分解生成碳酸钠;
(3)与实验Ⅲ相比,实验Ⅳ操作简单,对比性高;
(4)石灰水变浑,是因二氧化碳与石灰水反应生成碳酸钙;
(5)碳酸氢钠不稳定,便于对比可使碳酸氢钠受热温度低.
解答 解:(1)I中均与盐酸反应生成二氧化碳,石灰水均变浑浊;而Ⅱ中均与盐酸反应生成气体,但气球变大的快慢不同,则Ⅱ可鉴别,故答案为:Ⅱ;
(2)图Ⅲ、Ⅳ均为加热法鉴别,碳酸氢钠加热分解生成碳酸钠,反应为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)与实验Ⅲ相比,实验Ⅳ操作简单,对比性高,只有D符合,故答案为:D;
(4)石灰水变浑,是因二氧化碳与石灰水反应生成碳酸钙,石灰水变浑反应的离子方程式为CO2+Ca2++2OH-=CaCO3↓+H2O,
故答案为:CO2+Ca2++2OH-=CaCO3↓+H2O;
(5)碳酸氢钠不稳定,便于对比可使碳酸氢钠受热温度低,则试管B中装入物固体最好是NaHCO3,故答案为:NaHCO3.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、性质差异及反应与现象为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
14.高温下,某反应达平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$,恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| A. | 该反应的焓变为负值 | |
| B. | 升高温度,逆反应速率减小 | |
| C. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| D. | 该反应化学方程式为CO2+H2?CO+H2O |
9.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | lmol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 2L 0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为3NA | |
| D. | 标准状况下,11.2L苯中含有分子的数目为0.5NA |

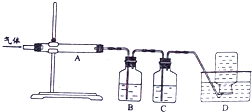
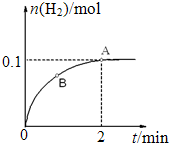
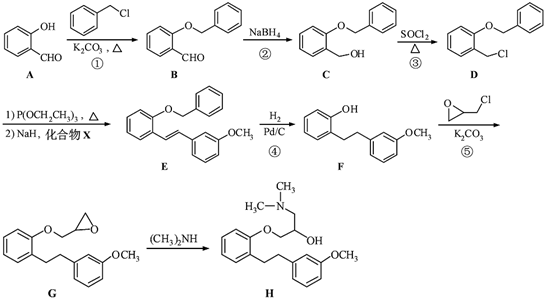
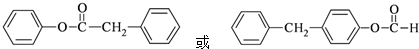 .
.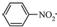 $→_{Pd/C}^{H_{2}}$
$→_{Pd/C}^{H_{2}}$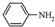 .化合物
.化合物 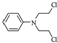 是合成抗癌药物美发伦的中间体,请写出以
是合成抗癌药物美发伦的中间体,请写出以  和
和 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
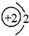 、O
、O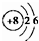 、Ca
、Ca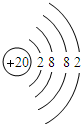 .
.