题目内容
9.NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | lmol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 2L 0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为3NA | |
| D. | 标准状况下,11.2L苯中含有分子的数目为0.5NA |
分析 A、亚铁离子和碘离子都能够被氯气氧化,1mol碘化亚铁完全反应消耗1.5mol氯气;
B、硫酸根带2个单位的负电荷;
C、Na2O2由2个钠离子和1个过氧根构成;
D、标况下,苯为液态.
解答 解:A、1molFeI2中含有1mol亚铁离子、2mol碘离子,完全反应需要消耗1.5mol氯气,转移了3mol电子,转移的电子数为3NA,故A错误;
B、2L0.5mol•L-1硫酸钾溶液中SO42-的物质的量n=CV=0.5mol/L×2L=1mol,而1个硫酸根带2个单位的负电荷,所以1mol硫酸钾中SO42-所带电荷数为2NA,但溶液中的阴离子除了SO42-还有OH-,故溶液中阴离子所带的电荷数大于2NA个,故B错误;
C、Na2O2由2个钠离子和1个过氧根构成,故1molNa2O2中共含3mol离子即3NA个,故C正确;
D、标况下,苯为液态,不能根据气体摩尔体积来计算其物质的量,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
17. 室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
 室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )
室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示.下列说法不正确的是( )| A. | Ⅱ表示的是滴定氨水的曲线,当V(HCl)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 当pH=7时,滴定氨水消耗的V(HCl)=20 mL,且c(NH4+)=c(Cl-) | |
| C. | 滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3•H2O) |
1.某物质的结构为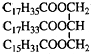 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )
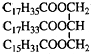 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )| A. | 一定条件下与氢气反应可以生成硬脂酸甘油酯 | |
| B. | 该物质不能使酸性KMnO4溶液褪色 | |
| C. | 与氢氧化钠溶液混合加热能得到肥皂的主要成分 | |
| D. | 与其互为同分异构且完全水解后产物相同的油脂还有三种 |
18.下列指定反应的离子方程式正确的是( )
| A. | Fe和足量稀硝酸反应Fe+2H+═Fe2++H2↑ | |
| B. | 将Fe(NO3)3溶液与少量HI混合:8H++2NO3-+6I-═4H2O+3I2+2NO↑ | |
| C. | 用过量氨水吸收SO2的反应:NH3•H2O+SO2═NH4++HSO3- | |
| D. | 少量Ca(OH)2和NaHCO3反应 Ca2++OH-+HCO3-═CaCO3↓+H2O |
19.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是( )
| A. | 向CuSO4溶液中加入适量铁粉 | |
| B. | 物质的量浓度为1:2、等体积的(NH4)2Fe(SO4)2与Ba(OH)2溶液 | |
| C. | 等物质的量的NaHCO3与Na2O2固体(隔绝空气) | |
| D. | 在NaBr溶液中通入过量氯气 |
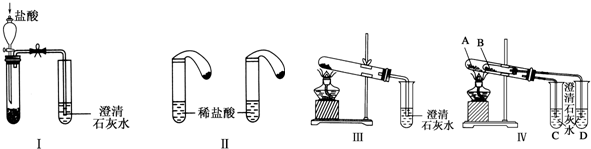
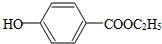 (一种常见化妆品的防霉剂),其生产过程如下图(反应条件没有全部注明):
(一种常见化妆品的防霉剂),其生产过程如下图(反应条件没有全部注明):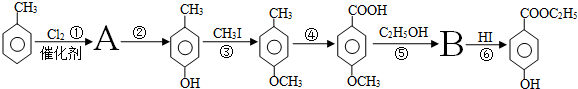
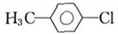 .
. .
. .
.
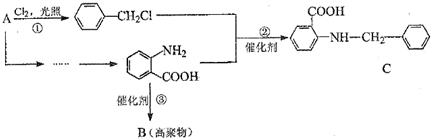
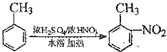

 (弱碱性,易被氧化)
(弱碱性,易被氧化)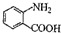 中官能团的名称氨基、羧基,②的反应类型是取代反应.
中官能团的名称氨基、羧基,②的反应类型是取代反应. 的同分异构体的结构简式
的同分异构体的结构简式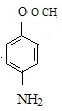 .
.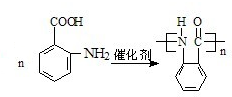 +nH2O.
+nH2O. 的合成路线.
的合成路线.