题目内容
【题目】制取聚合硫酸铁(PFS)的化学方程式如下
2FeSO4+H2O2+(1-n/2)H2SO4=Fe2(OH)n(SO4)(3-n/2)+(2-n)H2O,
下图是以回收废铁屑为原料制备PFS的一种工艺流程。
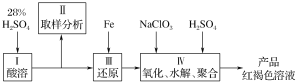
回答下列问题
(1)下列操作或描述正确的是________。
A.粉碎的目的是增大反应物接触面积,提高酸浸反应速率
B.酸浸中可以用硫酸、硝酸、盐酸等
C.反应釜中加入氧化剂,使Fe2+转化为Fe3+
D.减压蒸发的优点是降低蒸发温度,防止产物分解
(2)废铁屑使用前往往用________浸泡。
(3)废铁屑与酸发生多步反应,完成其中的化合反应的离子方程式______________________。
(4)聚合釜中溶液的pH必须控制在一定的范围内,目的是______________________。
(5)为了防止产物分解,必须采用减压蒸发,下列操作正确的是________。
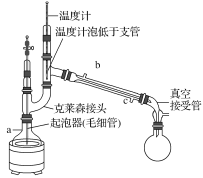
A.a为蒸馏烧瓶,b为冷凝管,c接自来水龙头
B.毛细管的作用和沸石相似,防止暴沸
C.随着温度计水银球高度提升,所得的气体的沸点升高
D.实验结束,先关闭冷凝管,再关闭真空泵
【答案】ACD )热的Na2CO3溶液 Fe+2Fe3+=3Fe2+ 促使Fe3+部分水解生成Fe2(OH)n(SO4)(3-n/2) BC
【解析】
(1)A、粉碎的目的是增大反应物接触面积,提高酸浸反应速率;
B.生成硫酸盐,只能用硫酸;
C.加入氧化剂使Fe2+转化为Fe3+;
D.减压蒸发的优点是降低蒸发温度,防止产物分解;
(2) Na2CO3水解显碱性;
(3)工业废铁屑中一部分已经生锈生成了Fe2O3,溶于酸有生成Fe3+;
(4)调节pH促使Fe3+部分水解生成Fe2(OH)n(SO4)(3-n/2);
(5)A.a为烧瓶,b为冷凝管,c接自来水龙头;
B.毛细管的作用和沸石相似,防止暴沸;
C.越往上温度越低,要达到相同的温度,收集到的气体的沸点升高;
D.实验结束,不要先关闭冷凝管,反应容器中还有气体产生,待冷却后关闭。
(1)A、粉碎的目的是增大反应物接触面积,提高酸浸反应速率,选项A正确;
B.根据所得产品可知,生成硫酸盐,只能用硫酸,选项B错误;
C.Fe2(OH)n(SO4)(3-n/2)中Fe是+3价,加入氧化剂使Fe2+转化为Fe3+,选项C正确;
D.减压蒸发的优点是降低蒸发温度,防止产物分解,选项D正确。
答案选ACD;
(2) Na2CO3水解显碱性,工业废铁屑中含有油污,使用前要用热的Na2CO3溶液浸泡除去;
(3)工业废铁屑中一部分已经生锈生成了Fe2O3,溶于酸有生成Fe3+,化合反应的离子方程式Fe+2Fe3+=3Fe2+;
(4)调节pH促使Fe3+部分水解生成Fe2(OH)n(SO4)(3-n/2),偏大偏小都会影响n的值;
(5)A.a为烧瓶,b为冷凝管,c接自来水龙头,选项A错误;
B.毛细管的作用和沸石相似,防止暴沸,选项B正确;
C.越往上温度越低,要达到相同的温度,收集到的气体的沸点升高,选项C正确;
D.实验结束,不要先关闭冷凝管,反应容器中还有气体产生,待冷却后关闭,选项D错误。
答案选BC。

 名校课堂系列答案
名校课堂系列答案【题目】已知N2(g)+3H2(g)![]() 2NH3(g) △H=92.4 kJ·mol-1,在温度相同、容积均为2 L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
2NH3(g) △H=92.4 kJ·mol-1,在温度相同、容积均为2 L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1 mol N2、3 mol H2 | 2 mol N2、6 mol H2 | 2 mol NH3 |
NH3的浓度(mol·L-1) | c1 | c2 | c3 |
反应的能量变化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
A.Q3+92.4c1=92.4B.α2+α3<1
C.2p1=2p3<p2D.达到平衡时丙容器中NH3的体积分数最大
【题目】已知:2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1。某温度下的平衡常数为400。此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表。下列说法中不正确的是( )
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1。某温度下的平衡常数为400。此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表。下列说法中不正确的是( )
物质 | CH3OH | CH3OCH3 | H2O |
c/mol·L-1 | 0.08 | 1.6 | 1.6 |
A. 此时刻反应达到平衡状态
B. 容器内压强不变时,说明反应达平衡状态
C. 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率不变
D. 平衡时,反应混合物的总能量降低40 kJ