题目内容
1.如图是部分短周期主族元素原子半径与原子序数的关系图.下列说法错误的是( )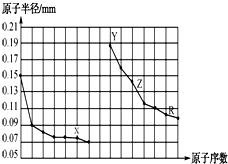
| A. | 同周期非金属元素中,X氢化物的沸点最高 | |
| B. | Y、Z的单质在空气中加热,均可发生燃烧反应 | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
分析 同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为Na元素,Z为Al元素,R为S元素,结合元素周期律与物质的性质等解答.
解答 解:同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为Na元素,Z为Al元素,R为S元素.
A.X为O元素,其氢化物的分子间存在氢键,所以同周期非金属元素中,X氢化物的沸点最高,故A正确;
B.Al在空气中不能燃烧,会有红热现象,故B错误;
C.Y、Z、R对应的最高价氧化物的水化物分别为:NaOH、Al(OH)3、H2SO4,氢氧化钠与硫酸发生中和反应,氢氧化铝属于两性氢氧化物,能与氢氧化钠、硫酸反应,故C正确;
D.工业上电解熔融的Al2O3冶炼Al,故D正确;
故选B.
点评 本题考查位置结构性质的关系及应用,题目难度中等,推断元素是解题的关键,根据原子半径变化规律结合原子序数进行推断,首先审题中要抓住“短周期主族元素”几个字.

练习册系列答案
相关题目
11.只用下列试剂中的一种,就能鉴别氢氧化钠溶液、氢氧化钙溶液和稀盐酸这三种无色溶液,它是( )
| A. | 酚酞试剂 | B. | BaCl2溶液 | C. | 石蕊试剂 | D. | Na2CO3溶液 |
9.在盛有稀硫酸的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
| A. | 铜片上发生了还原反应 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 正极有O2逸出 | |
| D. | 正极附近的SO42-离子浓度逐渐增大 |
16. 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的四种溶液:pH由小到大排列的顺序是a<d<c<b(用编号填写).a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol•L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$ E.$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$
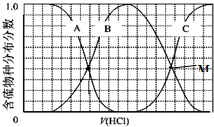
(3)硫单质及其化合物在工农业生产中有着重要的应用.向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸 至过量.其中H2S、HS-、S2-的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出).试分析:
①B曲线代表HS-分数变化(用微粒符号表示);滴加过程中,溶液中一定成立:c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]或c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);.
②M点,溶液中主要涉及的离子方程式2S2-+3H+=HS-+H2S.
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平 衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L-1的四种溶液:pH由小到大排列的顺序是a<d<c<b(用编号填写).a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol•L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$ E.$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$
(3)硫单质及其化合物在工农业生产中有着重要的应用.向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸 至过量.其中H2S、HS-、S2-的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出).试分析:
①B曲线代表HS-分数变化(用微粒符号表示);滴加过程中,溶液中一定成立:c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]或c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);.
②M点,溶液中主要涉及的离子方程式2S2-+3H+=HS-+H2S.
13.对于在同一容器中进行的反应C+O2═CO2,下列说法不正确的是( )
| A. | 将碳块磨成粉末可以加快反应速率 | |
| B. | 升高温度一般可以加快反应速率 | |
| C. | 容器体积不变时,向其中充入N2,反应速率不变 | |
| D. | 增加碳的量可以加快反应速率 |
15.下列说法正确的是( )
| A. | 强酸跟强碱的反应热一定是中和热 | |
| B. | 1molC完全燃烧放热383.3kJ,其热化学方程为:C+O2═CO2 △H=-383.3kJ•mol-1 | |
| C. | 在稀溶液中,酸与碱发生中和反应生成1mol H2O时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为:H+(aq)+OH-(aq)═H2O(l);△H=57.3KJ•mol-1 |