题目内容
15.下列说法正确的是( )| A. | 强酸跟强碱的反应热一定是中和热 | |
| B. | 1molC完全燃烧放热383.3kJ,其热化学方程为:C+O2═CO2 △H=-383.3kJ•mol-1 | |
| C. | 在稀溶液中,酸与碱发生中和反应生成1mol H2O时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为:H+(aq)+OH-(aq)═H2O(l);△H=57.3KJ•mol-1 |
分析 A、中和热是强酸、强碱稀溶液全部反应生成1mol水放出的热量;
B、热化学方程式中物质聚集状态未标注;
C、中和热是强酸、强碱稀溶液全部反应生成1mol水放出的热量;
D、中和反应是放热反应,反应焓变为负值.
解答 解:A、中和热是强酸、强碱稀溶液全部反应生成1mol水放出的热量,若是浓硫酸和氢氧化钠溶液反应过程中除中和热还有溶解热,不是中和热,故A错误;
B、热化学方程式中物质聚集状态未标注,1molC完全燃烧放热383.3kJ,其热化学方程为:C(s)+O2(g)═CO2 (g)△H=-383.3kJ•mol-1,故B错误;
C、中和热是强酸、强碱稀溶液全部反应生成1mol水放出的热量,在稀溶液中,酸与碱发生中和反应生成1mol H2O时的反应热叫做中和热,故C正确;
D、中和反应是放热反应,反应焓变为负值,表示中和热的离子方程式为:H+(aq)+OH-(aq)═H2O(l),△H=-57.3KJ•mol-1,故D错误;
故选C.
点评 本题考查了中和热、燃烧热概念实质,热化学方程式书写方法,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
1.如图是部分短周期主族元素原子半径与原子序数的关系图.下列说法错误的是( )
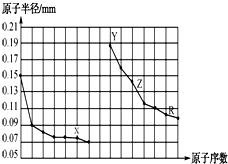

| A. | 同周期非金属元素中,X氢化物的沸点最高 | |
| B. | Y、Z的单质在空气中加热,均可发生燃烧反应 | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
6.相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)
△H=-197kJ•mol-l.实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是( )
△H=-197kJ•mol-l.实验测得起始、平衡时的有关数据如下表:
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO2 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q2 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 三个容器中反应的平衡常数不相等 | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$ mol/(L•min) |
3.在下列各说法中,正确的是( )
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | △H>0表示放热反应,△H<0表示吸热反应 | |
| C. | 酸碱中和时放出的热叫做中和热 | |
| D. | 1mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
20.在容积相同的两个密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol及bmol HI(a>b),可逆反应2HI(g)?H2(g)+I2(g)达到平衡后,下列说法正确的是( )
| A. | 开始时A容器中的反应速率大于B容器中的反应速率 | |
| B. | 平衡时c(I2)A=c(I2)B | |
| C. | HI的平衡分解率:αA>αB | |
| D. | 平衡时,I2蒸气在混合气体中的体积分数:A容器>B容器 |
4.铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛.铁还有很多重要的化合物及其化学反应.
如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)△H
(1)上述反应的平衡常数表达式K=$\frac{{c}^{4}({H}_{2})}{{c}^{4}({H}_{2}O)}$.
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s)△H1=-1118.4kJ•mol-1
②2H2(g)+O2(g)=2H2O(g)△H2=-483.8kJ•mol-1
③2H2(g)+O2(g)=2H2O(l)△H3=-571.8kJ•mol-1
则△H=-150.8kJ•mol-1.
(3)在t℃时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
①甲容器中H2O的平衡转化率为33.3%(结果保留一位小数).
②下列说法正确的是BC (填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
若在达平衡后的装置中继续加入A、B、C三种状况下的各物质,见表:
当上述可逆反应再一次达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是B>C>A(用A、B、C表示).
如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)△H
(1)上述反应的平衡常数表达式K=$\frac{{c}^{4}({H}_{2})}{{c}^{4}({H}_{2}O)}$.
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s)△H1=-1118.4kJ•mol-1
②2H2(g)+O2(g)=2H2O(g)△H2=-483.8kJ•mol-1
③2H2(g)+O2(g)=2H2O(l)△H3=-571.8kJ•mol-1
则△H=-150.8kJ•mol-1.
(3)在t℃时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe | H2O(g) | Fe3O4 | H2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
②下列说法正确的是BC (填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
| Fe | H2O(g) | Fe3O4 | H2 | |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| Fe | H2O(g) | Fe3O4 | H2 | |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1 | 4 |
| C/mol | m | n | p | q |
5.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 明矾能够净水,是因为明矾水解生成的Al(OH)3胶体能杀死水中的细菌 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 提倡人们购物时不用塑料袋,是为了节约资源,减少白色污染 |