题目内容
9.在盛有稀硫酸的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )| A. | 铜片上发生了还原反应 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 正极有O2逸出 | |
| D. | 正极附近的SO42-离子浓度逐渐增大 |
分析 铜-锌-稀硫酸原电池中,活泼金属锌作负极,铜作正极;负极上锌失电子生成锌离子,正极上氢离子得电子生成氢气;溶液中阴离子向负极移动,阳离子向正极移动;由此分析解答.
解答 解:A、铜-锌-稀硫酸原电池中,活泼金属锌作负极,铜作正极发生还原反应,故A正确;
B、铜-锌-稀硫酸原电池中,活泼金属锌作负极,铜作正极,原电池放电时,电子从负极锌沿导线流向正极铜,故B错误;
C、正极上氢离子得电子生成氢气,故C错误;
D、该原电池放电时,溶液中阴离子向负极移动,阳离子向正极移动,所以硫酸根离子向负极移动,负极附近SO42-浓度逐渐增大,故D错误;
故选:A.
点评 本题考查了原电池原理,难度不大,易错点为:判断溶液中阴阳离子的移动方向.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
19. 某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
 某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )
某密闭容器中发生如下反应:2X(g)+Y(g)?Z(g);△H<0 如图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5 时刻外界条件有所改变,但都没有改变各物质的用量.则下列说法中不正确的是( )| A. | t3 时降低了压强 | |
| B. | t5 时提高了温度 | |
| C. | t1-t2 时该反应的平衡常数小于 t6时反应的平衡常数 | |
| D. | t6 时刻后反应物的转化率最低 |
20.下列物质属于同位素的是( )
| A. | H2O和H2O2 | B. | 11H、21H、31H | C. | O2与O3 | D. | 11H2和21D2 |
17.下列实验操作正确的是( )
| A. | 用蒸发方法使NaCl从溶液中析出时,应边加热边搅拌直至溶液蒸干 | |
| B. | 用10mL量筒量取8.58mL蒸馏水 | |
| C. | 容量瓶定容时观察液面时俯视,会使配得的溶液浓度偏大 | |
| D. | 用酒精萃取碘水中的I2 |
4. 1.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-.现进行如下实验:
1.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-.现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
Ⅲ.向Ⅱ中所得溶液中加入BaCl2溶液,有白色沉淀生成
Ⅳ.向Ⅱ中所得溶液中加入过量浓氨水,仅有红褪色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成
请回答下列问题:
(1)该废水一定含有的离子是Fe2+、Cu2+、NO3-、SO42-;
(2)实验Ⅱ中加入盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)过滤除去Ⅳ中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1:4,其离子方程式为Al+NO3-+OH-AlO2-+NH3+N2+H2O(未配平).若除去0.2molNO3-,消耗铝9.6g.
2.某混合液中,可能大量含有的离子如表:
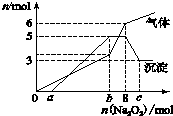
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示:
(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)请写出沉淀减少的离子方程式Al(OH)3+OH-═AlO2-+2H2O.
 1.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-.现进行如下实验:
1.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-.现进行如下实验:Ⅰ.取少量溶液,加入KSCN溶液,无明显变化
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
Ⅲ.向Ⅱ中所得溶液中加入BaCl2溶液,有白色沉淀生成
Ⅳ.向Ⅱ中所得溶液中加入过量浓氨水,仅有红褪色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成
请回答下列问题:
(1)该废水一定含有的离子是Fe2+、Cu2+、NO3-、SO42-;
(2)实验Ⅱ中加入盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)过滤除去Ⅳ中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1:4,其离子方程式为Al+NO3-+OH-AlO2-+NH3+N2+H2O(未配平).若除去0.2molNO3-,消耗铝9.6g.
2.某混合液中,可能大量含有的离子如表:
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、Br-、OH-、CO32-、AlO2- |
(1)该溶液中一定含有的阳离子是H+、Al3+、NH4+、Mg2+,其对应物质的量浓度之比为2:2:2:3,溶液中一定不存在的阴离子是OH-、CO32-、AlO2-.
(2)请写出沉淀减少的离子方程式Al(OH)3+OH-═AlO2-+2H2O.
14.在标准状况下,将aLNH3完全溶于水得到V mL氨水,溶液的密度为ρg/cm3,溶质的质量分数为ω,溶质的物质的量浓度为cmol/L.下列叙述中正确的是( )
| A. | ω=$\frac{35a}{22.4Vρ}$×100% | |
| B. | c=$\frac{1000a}{22.4Vρ}$×100%mol/L | |
| C. | 上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| D. | 上述氨水中再加入V mL水后,所得溶液的质量分数大于0.5ω |
1.如图是部分短周期主族元素原子半径与原子序数的关系图.下列说法错误的是( )
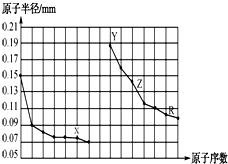

| A. | 同周期非金属元素中,X氢化物的沸点最高 | |
| B. | Y、Z的单质在空气中加热,均可发生燃烧反应 | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
3.在下列各说法中,正确的是( )
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | △H>0表示放热反应,△H<0表示吸热反应 | |
| C. | 酸碱中和时放出的热叫做中和热 | |
| D. | 1mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |