题目内容
【题目】在试管中进行下列实验,现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向硫酸铜水溶液中逐滴加入氨水 | 先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液 |
B | 向I2的CCl4溶液中加入浓KI溶液,振荡 | 溶液紫红色变浅 |
C | 向橙色的K2Cr2O7溶液中加入10滴浓硫酸,振荡 | 溶液由橙色变为黄色 |
D | 向饱和硼酸溶液中加入Na2CO3溶液 | 无明显现象 |
A.AB.BC.CD.D
【答案】C
【解析】
A. 向硫酸铜水溶液中逐滴加入氨水,先产生蓝色沉淀氢氧化铜沉淀,然后溶解,最后得到深蓝色硫酸四氨合铜透明溶液,故A正确;
B. 根据 I2+ I-![]() I3-,向I2的CCl4溶液中加入浓KI溶液,振荡生成I3-,平衡正向移动,因此溶液紫红色变浅,故B正确;
I3-,向I2的CCl4溶液中加入浓KI溶液,振荡生成I3-,平衡正向移动,因此溶液紫红色变浅,故B正确;
C. 向橙色的K2Cr2O7溶液中加入10滴浓硫酸,振荡,2CrO42 + 2 H+![]() Cr2O72 + H2O,因此平衡向生成Cr2O72方向移动,溶液橙色加深,故C错误;
Cr2O72 + H2O,因此平衡向生成Cr2O72方向移动,溶液橙色加深,故C错误;
D. 向饱和硼酸溶液中加入Na2CO3溶液,不反应,因此无明显现象,故D正确。
综上所述,答案为C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
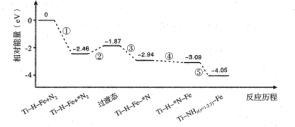
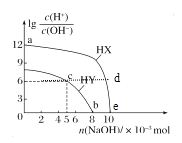
小学生10分钟应用题系列答案【题目】中国是稀土资源大国,稀土是化学元素周期表中镧系元素和钪、钇共十七种金属元素的总称,被誉为“万能之土”。某小组以钇矿石(Y2FeBe2Si2O10)为主要原料制备氧化钇(Y2O3)和铍的流程(部分条件和产物省略)如图所示:
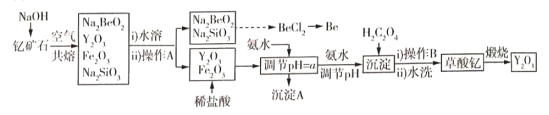
已知部分信息如下:
①铍、铝的单质及其化合物的化学性质相似;
②稀土元素都是活泼金属,性质相似,常见化合价为+3;
③Fe3+ Y3+形成的氢氧化物沉淀的pH范围如表所示:
离子 | Fe3+ | Y3+ |
开始沉淀的PH | 2.1 | 6.0 |
完全沉淀的PH | 3.1 | 8.3 |
请回答下列问题:
(1)沉淀A的主要成分是______(填化学式);操作A的名称是____________________。
(2)钇矿石与氢氧化钠共熔反应中的氧化产物为__________;写出加入草酸生成沉淀的离子方程式:___________;草酸钇隔绝空气煅烧的方程式______________。
(3)调节pH=a,则a的范围为______________。
(4)已知常温下;K[Y(OH)3]=1.0×10-23。Y3++3H2O=Y(OH)3+3H+平衡常数为K,则pK=-lgK=_____。
(5)叙述由Na2SiO3和Na2BeO3溶液制取BeCl2固体的过程:_______________。
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
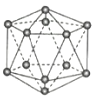
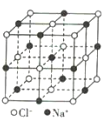
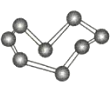
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键