题目内容
【题目】下列物质的性质比较,结论错误的是
A.硬度:金刚石>碳化硅>晶体硅
B.离子半径:S2->Cl->Na+>O2-
C.熔点:NaF>NaCl>NaBr>NaI
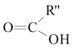
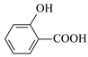
D.沸点:![]() >
>
【答案】B
【解析】
A. 键长C—C>C—Si>Si—Si,键长越短,键能越大,硬度越大,因此硬度:金刚石>碳化硅>晶体硅,故A正确;
B. 根据层多径大,同电子层结构核多径小,因此离子半径:S2>Cl->O2>Na+,故B错误;
C. 离子半径F-<Cl-<Br-<I-,根据键长越短,键能越大,晶格能越大,熔沸点越高,因此熔点:NaF>NaCl>NaBr>NaI,故C正确;
D. ![]() 存在分子间氢键,
存在分子间氢键,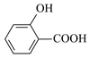 存在分子内氢键沸点,分子间氢键影响熔沸点升高,分子内氢键影响熔沸点降低,因此沸点:
存在分子内氢键沸点,分子间氢键影响熔沸点升高,分子内氢键影响熔沸点降低,因此沸点:![]() >
> ,故D正确。
,故D正确。
综上所述,答案为B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目