题目内容
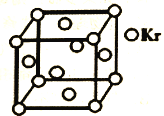
【题目】如图为 NaCl 晶胞结构示意图(晶胞边长为 a nm)。
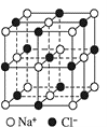

(1)能准确证明其是晶体的方法是_____
(2)晶体中,Na+位于Cl-所围成的正_____面体的体心, 该多面体的边长是_____nm。
(3)晶体中,在每个Na+的周围与它最近且等距离的 Na+共有_____个。
(4)Na+半径与 Cl-半径的比值是_________(保留小数点后三位, ![]() =1.414。
=1.414。
(5)在 1413℃时,NaCl 晶体转变成氯化钠气体。现有 5.85 g NaCl 晶体,使其汽化,测得气体体积为 1.12 L(已换算为标准状况)。则此时氯化钠气体的分子________。
【答案】X-射线衍射法 或 X-射线衍射实验 八 ![]() 12 0.414 Na2Cl2 或 (NaCl)2
12 0.414 Na2Cl2 或 (NaCl)2
【解析】
(1)X-射线衍射法或X-射线衍射实验能准确确定某种物质是晶体;
(2)晶体中,以Na+为中心在它的上下前后左右有6个Cl-,Na+位于Cl-所围成的正八面体的体心,如图 该多面体的边长=图中对角线长的一半=
该多面体的边长=图中对角线长的一半=![]() nm;
nm;
(3)晶体中,以Na+为中心的三个垂直的面上各有4个Na+,在每个Na+的周围与它最近且等距离的 Na+共有12个。
(4)根据 确定NaCl晶体中阴阳离子的最短距离;
确定NaCl晶体中阴阳离子的最短距离;
(5)M=m/n=mVm/V,根据摩尔质量确定其化学式。
(1)能准确证明其是晶体的方法是X-射线衍射法或X-射线衍射实验;
(2)晶体中,以Na+为中心在它的上下前后左右有6个Cl-,Na+位于Cl-所围成的正八面体的体心,如图 该多面体的边长=图中对角线长的一半=
该多面体的边长=图中对角线长的一半=![]() nm;
nm;
(3)晶体中,以Na+为中心的三个垂直的面上各有4个Na+,在每个Na+的周围与它最近且等距离的 Na+共有12个。
(4)根据图 ,NaCl晶体中阴阳离子的最短距离为a的一半即a/2,氯离子的半径为对角线的1/4,即为
,NaCl晶体中阴阳离子的最短距离为a的一半即a/2,氯离子的半径为对角线的1/4,即为![]() ,由图
,由图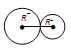 ,钠离子的半径为(a/2-
,钠离子的半径为(a/2-![]() ),所以Na+离子半径与Cl-离子半径之比为 r+/r-=
),所以Na+离子半径与Cl-离子半径之比为 r+/r-=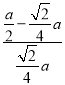 =0.414;
=0.414;
(5)1mol氯化钠的质量=1mol×58.8g·mol-1=58.5g,标况下,气体体积为11.2L的氯化钠的物质的量=11.2L/22.4L·mol-1=0.5mol,M=58.5g/0.5mol=117g·mol-1,所以氯化钠气体的分子式为Na2Cl2。

 阅读快车系列答案
阅读快车系列答案【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X(g)+3Y(g)2Z(g),其平衡常数为1600
C.改变温度可以改变此反应的平衡常数
D.改变压强,平衡常数不变,平衡不移动