题目内容
【题目】将在空气中暴露一段时间后的氢氧化钠固体样本溶于水得溶液A,将所得溶液中逐滴滴加稀硫酸至过量,生成的二氧化碳体积(标准状况下)与加入稀硫酸体积关系如图所示.
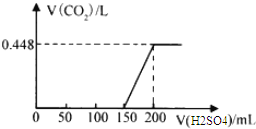
已知:在碳酸钠溶液中逐滴加入稀硫酸反应按以下步骤进行:
①CO32-+H+═HCO3- ②H++HCO3-═CO2↑+H2
试计算:
(1)溶液A中滴加硫酸的体积在0-150mL间无CO2气体生成的原因是(用离子方程式表示)______.
(2)硫酸滴加至150mL时,此时溶液中溶质主要成分为(写化学式)______.
(3)溶液A中碳酸钠的质量为______g.
(4)硫酸的物质的量浓度为______mol/L.
(5)该样品中Na2CO3与NaOH物质的量之比为______.
【答案】 0-150mL间发生2NaOH+H2SO4=Na2SO4+2H2O、2Na2CO3+H2SO4=Na2SO4+2NaHCO3 Na2SO4和NaHCO3 2.12g 0.2mol/L 2:1
【解析】(1)因为碳酸钠与硫酸反应生成碳酸氢钠,碳酸氢钠与硫酸反应生成二氧化碳,两反应消耗硫酸的物质的量相等,由图可知V(H2SO4)在0~100mL区间内发生反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;在100~150mL区间内发生反应的化学方程式为2Na2CO3+H2SO4=Na2SO4+2NaHCO3;(2)由(1)知:硫酸滴加至150mL时,此时溶液中溶质主要成分为Na2SO4和NaHCO3;(3)根据碳守恒可知:Na2CO3~CO2,而二氧化碳的体积为0.448L,所以碳酸钠的物质的量为:0.448L/22.4L·mol-1=0.02mol,则质量为:0.02mol×106g·mol-1=2.12g;(4)加入150mL~200mL硫酸,发生反应:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O,n(H2SO4)=0.02mol/2=0.01mol,则c=n/V=0.01mol/0.05L=0.2mol·L-1;(5)加入200mL硫酸时,生成0.448L二氧化碳,此时溶液中溶质为Na2SO4,由硫酸根离子守恒计算n(Na2SO4)=0.2L×0.2mol·L-1=0.04mol,根据碳元素守恒n(Na2CO3)=n(CO2)=0.02mol,根据钠离子守恒n(NaOH)=2n(Na2SO4)-2n(Na2CO3)=0.08mol-0.02mol×2=0.04mol,该样品中NaOH与Na2CO3物质的量之比=0.04mol:0.02mol=2:1。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案