题目内容
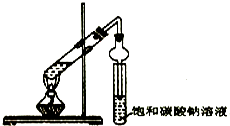
【题目】氢氧化铁胶体制备步骤如下:
①用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
②向烧杯中逐滴加入饱和FeCl3溶液;
③继续煮沸至液体是透明的红褐色,即得Fe(OH)3胶体.
回答下列问题:
(1)写出制备Fe(OH)3胶体的化学方程式;
(2)如何确定你制备胶体是否成功?;
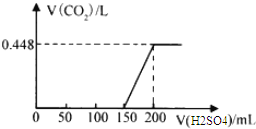
(3)若向Fe(OH)3胶体中逐滴加入H2SO4溶液至过量会出现的现象: .
【答案】
(1)FeCl3+3H2O ![]() Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(2)出现丁达尔效应说明胶体制备成功
(3)先出现红褐色沉淀,随后沉淀溶解
【解析】解:(1)制备Fe(OH)3胶体是利用了Fe3+在溶液中结合了水中的OH﹣ , 生成了Fe(OH)3(胶体)和HCl,化学方程式为:FeCl3+3H2O ![]() Fe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2O
Fe(OH)3(胶体)+3HCl,故答案为:FeCl3+3H2O ![]() Fe(OH)3(胶体)+3HCl;(2)胶体区别于其他分散系的特有的性质为丁达尔效应,故要判断胶体是否制备成功,可以用丁达尔效应来判断,当可见光通过时出现一条光亮的通路,
Fe(OH)3(胶体)+3HCl;(2)胶体区别于其他分散系的特有的性质为丁达尔效应,故要判断胶体是否制备成功,可以用丁达尔效应来判断,当可见光通过时出现一条光亮的通路,
故答案为:出现丁达尔效应说明胶体制备成功;(3)向Fe(OH)3胶体中逐滴加入H2SO4溶液至过量,电解质H2SO4电离出的SO42﹣使Fe(OH)3胶体发生聚沉,生成红褐色沉淀,氢氧化铁胶体聚沉后会产生氢氧化铁沉淀,继续加入硫酸,会发生酸碱中和反应,生成氯化铁和水,此反应的离子方程式是Fe(OH)3+3H+═Fe3++3H2O,出现的现象为:先出现红褐色沉淀,随后沉淀溶解,
故答案为:先出现红褐色沉淀,随后沉淀溶解.
(1)制备Fe(OH)3胶体是利用了Fe3+在溶液中的水解;(2)根据胶体的独有的性质﹣﹣丁达尔效应来分析;(3)根据胶体的性质判断,加入稀硫酸产生聚沉现象;氢氧化铁胶体聚沉后会产生氢氧化铁沉淀,硫酸和氢氧化铁沉淀反应,生成硫酸铁和水.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如表:
按下列合成步骤回答问题:
苯 | 溴 | 溴苯 | |
密度/gcm﹣3 | 0.88 | 3.10 | 1.50 |
沸点/°C | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白色烟雾产生,是因为生成了气体.继续滴加至液溴滴完.装置d的作用是
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,下列操作中必须的是(填入正确选项前的字母);
A.重结晶
B.过滤
C.蒸馏
D.萃取
(4)在该实验中,a的容积最适合的是(填入正确选项前的字母).
A.25mL B.50mL C.250mL D.500mL
(5)写出a中反应的主要有机化学方程式