题目内容
【题目】某同学为了检验浓硫酸与木炭粉在加热条件下反应:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。产生的所有气体产物,选用了如图所示实验装置。
CO2↑+2SO2↑+2H2O。产生的所有气体产物,选用了如图所示实验装置。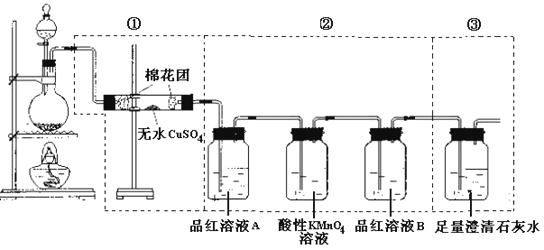
(1)①中无水硫酸铜的作用是___。
(2)②中酸性KMnO4溶液的作用是__。
(3)②中两次用到品红溶液,A的作用是___,B的作用分别是___。
【答案】检验反应生成的水蒸气 除去混合气体中的SO2 检验生成的的SO2 检验SO2是否除尽
【解析】
木炭粉与浓硫酸反应化学方程式为:C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O,用无水硫酸铜检验水蒸气,用品红溶液检验二氧化硫,用澄清石灰水检验二氧化碳,由于二氧化硫与澄清石灰水也产生白色沉淀,故检验二氧化碳前需要除去二氧化硫,品红溶液A检验SO2,通过酸性高锰酸钾溶液除去SO2,品红溶液B检验二氧化硫是否除尽,品红溶液B不褪色,澄清石灰水变浑浊,说明生成二氧化碳。
2SO2↑+CO2↑+2H2O,用无水硫酸铜检验水蒸气,用品红溶液检验二氧化硫,用澄清石灰水检验二氧化碳,由于二氧化硫与澄清石灰水也产生白色沉淀,故检验二氧化碳前需要除去二氧化硫,品红溶液A检验SO2,通过酸性高锰酸钾溶液除去SO2,品红溶液B检验二氧化硫是否除尽,品红溶液B不褪色,澄清石灰水变浑浊,说明生成二氧化碳。
(1)实验利用白色硫酸铜(CuSO4)遇到水变为蓝色(CuSO45H2O),证明含有水蒸气,所以①中无水硫酸铜的作用是检验反应生成的H2O,故答案为:检验反应生成的H2O;
(2)因SO2和CO2都能使石灰水变浑浊,因此要想检验出CO2,就要先把SO2检验了,并除掉SO2,这样石灰水变浑浊才能说明有CO2,所以酸性高锰酸钾溶液是除去混合气中的二氧化硫,反应为5SO2+2MnO4+2H2O=5SO42+2Mn2++4H+,故答案为:除去混合气中的SO2;
(3)②中两次用到品红溶液,品红溶液A检验生成的SO2气体,通过酸性高锰酸钾溶液除去SO2,品红溶液B是检验SO2是否除尽,故答案为:检验生成的的SO2;检验SO2是否除尽。

练习册系列答案
相关题目