题目内容
【题目】已知CaCO3和盐酸反应的化学方程式为CaCO3(s)+2HCl===CaCl2+H2O+CO2↑,下列措施中可使生成CO2的速率加快的是(不考虑CaCO3与盐酸接触面积改变的影响)
A. 加大CaCO3的量 B. 加大盐酸的浓度
C. 加大盐酸的量 D. 减小CaCl2的浓度
【答案】B
【解析】A. 碳酸钙是固体,加大CaCO3的量反应速率不变,A错误;B. 加大盐酸的浓度加快反应速率,B正确;C. 加大盐酸的量盐酸浓度不变,反应速率不变,C错误;D. 减小CaCl2的浓度氢离子浓度不变,反应速率不变,D错误,答案选B。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
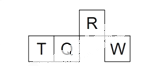
【题目】下表是元素周期表的前四周期,请回答有关问题:(相关均用具体化学用语回答)
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ | ||||||
(1)元素⑤⑥⑦的简单离子半径大小顺序__________;②在元素周期表位置________;③的简单氢化物和⑧的氢化物混合形成的化合物电子式__________。
(2)⑤其最高价氧化物水合物和⑥的最高价氧化物反应的离子方程式_______
(3)用电子式表示元素①和⑧形成的化合物的形成过程__________。
(4)④、⑧、⑩的氢化物沸点最高的是__________,原因是__________。
(5)由②和①组成最简单物质与O2和⑨的最高价氧化物对应的水化物的水溶液组成燃料电池,写出电池的负极反应式__________。