题目内容
17.某化合物,其组成中没有C、H、O三种元素.这种化合物可能属于( )| A. | 酸 | B. | 碱 | C. | 盐 | D. | 有机物 |
分析 可根据酸、碱、盐的概念和组成元素进行分析判断.有机物含有碳氢元素,大部分含有氧元素.
解答 解:酸是指电离时生成的阳离子全部是氢离子的化合物.所以酸中必含氢元素.
碱是指电离时生成的阴离子全部是氢氧根离子的化合物.所以碱中必含氢元素和氧元素.
有机物含有碳氢元素.所以组成中没有C、H、O三种元素,一定不会是酸、碱和有机物.
故选C.
点评 要想解答好这类题目,要理解和熟记有机物、酸、碱和盐的概念,以及与之相关的知识.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
7.在下列给定条件的各溶液中,一定能大量共存的离子组是( )
| A. | 室温下$\frac{{K}_{W}}{c({H}^{+})}$=10-13 mol•L-1的溶液中:NH4+、Mg2+、NO3-、SO42- | |
| B. | 含有0.1 mol•L-1 Fe3+的溶液中:K+、Mg2+、SCN-、NO3- | |
| C. | 加入Al能放出H2的溶液中:NH4+、K+、Cl-、HCO3- | |
| D. | 在H+、Na+、SO42-浓度均为0.1 mol•L-1的溶液中:K+、SiO32-、Cl-、CH3COO- |
8.下列说法中,错误的是( )
| A. | 石油分馏所得的馏分仍是混合物 | |
| B. | 天然气的主要成分是甲烷、乙烯等气体 | |
| C. | 煤焦油经分馏可得苯和甲苯 | |
| D. | 含C20以上的重油经催化裂化可得汽油、柴油等轻质油 |
12.碱性锌锰电池的总反应是:Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2,电解质是KOH.下列说法正确的是( )
| A. | MnO2发生了氧化反应 | |
| B. | MnOOH中Mn元素的化合价为+3 | |
| C. | 反应消耗 0.65g Zn,有0.01 mol电子发生转移 | |
| D. | 碱性锌锰电池是一种高效、环境友好的发电装置 |
9.欲除去小苏打溶液中的苏打杂质,加入的物质最宜选用( )
| A. | 二氧化碳 | B. | 盐酸 | C. | 碳酸氢钙 | D. | 氢氧化钙 |
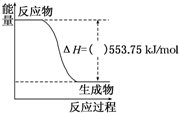 2011年深圳大运会“虹”火炬采用丙烷为燃料.丙烷热值较高,污染较小,是一种优良的燃料.试回答下列问题:
2011年深圳大运会“虹”火炬采用丙烷为燃料.丙烷热值较高,污染较小,是一种优良的燃料.试回答下列问题: