题目内容
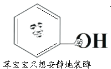
【题目】![]() 是制备硫酸的重要反应。下列说法正确的是
是制备硫酸的重要反应。下列说法正确的是
A.加入催化剂,反应速率加快,反应的![]() 变大
变大
B.将平衡后的混合气体用浓硫酸吸收,剩余的气体只有![]()
C.98%的浓硫酸用等体积的水稀释后,硫酸的质量分数为49%
D.若以稀硫酸为电解液,将该反应设计成原电池,放电过程中负极附近溶液的pH不断减小
【答案】D
【解析】
A、加入催化剂,反应速率加快,但反应热只与反应物和生成物的总能量有关,故△H不变,A错误;
B、平衡混合物中除SO3和O2外还有SO2,浓硫酸只能吸收SO3,B错误;
C、浓硫酸的密度大于水,故用等体积的水稀释后,溶液的质量小于原溶液的2倍,质量分数>原来的一半,C错误;
D、以该反应设计的原电池,负极上的反应为SO2变为SO3,SO3与水生成硫酸,使氢离子浓度升高,pH减小,D正确;
故答案选D。

练习册系列答案
相关题目