题目内容
【题目】已知: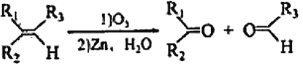 ,其中R1、R2、R3为烷基。现有一种五元环状内酯F的合成路线如下(C~G均表示一种有机化合物):
,其中R1、R2、R3为烷基。现有一种五元环状内酯F的合成路线如下(C~G均表示一种有机化合物):
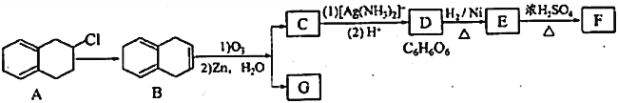
回答下列问题:
(1)化合物B的分子式为________,G中含有的官能团名称是_________________________________。
(2)由A→B所需的反应试剂和反应条件为___________________________。
(3)化合物E的系统命名为________________________________________。
(4)根据已知信息,由B生成C和G的的化学方程式为______________________________________。
(5)同时满足下列条件的G的同分异构体一共有____________________种(不含顺反异构)。
(I)与NaHCO3反应产生气体 (II)能使溴水褪色
(6)根据题给信息,写出用2,3—二甲基—2—丁烯制备丙烯的合成路线(其他试剂任选)_________。
【答案】C10H12 醛基 NaOH的醇溶液加热 消去反应 3,4—二羟基已二酸  3
3 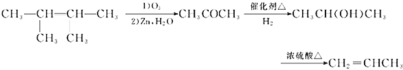
【解析】
根据A、B的结构简式,可知A在氢氧化钠的醇溶液中加热发生消去反应生成B;结合![]() ,可知B在相同条件下生成
,可知B在相同条件下生成![]() 和
和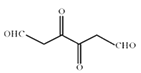 ,结合D的分子式是C6H6O6,可知C是
,结合D的分子式是C6H6O6,可知C是 、G是
、G是![]() ;
;  能被银氨溶液氧化为
能被银氨溶液氧化为 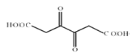 ,D是
,D是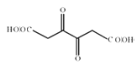 ,
,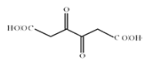 与氢气发生加成反应生成E,E是
与氢气发生加成反应生成E,E是![]() 。
。
(1)根据化合物B的结构简式,可知B的分子式是C10H12;G是![]() ,含有的官能团名称是醛基;(2)
,含有的官能团名称是醛基;(2)![]() 在氢氧化钠的醇溶液中加热发生消去反应生成
在氢氧化钠的醇溶液中加热发生消去反应生成![]() 。 (3)化合物E是
。 (3)化合物E是![]() ,系统命名为3,4 —二羟基已二酸。 (4)根据已知信息,由
,系统命名为3,4 —二羟基已二酸。 (4)根据已知信息,由![]() 生成
生成![]() 和
和 ,的的化学方程式为
,的的化学方程式为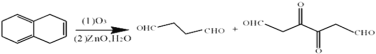 。 (5)与NaHCO3反应产生气体说明含有羧基,能使溴水褪色说明含有碳碳双键;同时满足条件的
。 (5)与NaHCO3反应产生气体说明含有羧基,能使溴水褪色说明含有碳碳双键;同时满足条件的![]() 的同分异构体有
的同分异构体有![]() 、
、![]() 、
、![]() ,共3种; (6) 2,3—二甲基—2—丁烯发生氧化反应,生成丙酮,丙酮再还原为2-丙醇,2-丙醇发生消去反应可生成丙烯,合成路线为
,共3种; (6) 2,3—二甲基—2—丁烯发生氧化反应,生成丙酮,丙酮再还原为2-丙醇,2-丙醇发生消去反应可生成丙烯,合成路线为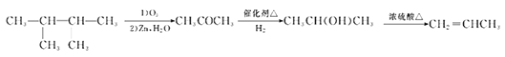 。
。

 寒假学与练系列答案
寒假学与练系列答案【题目】按要求回答问题:
(1)除去下列表格物质中的杂质(括号中是杂质),从所给试剂及操作方法中选出合适的药品及方法(填序号):
除杂试剂:A.溴水 B.饱和碳酸钠溶液 C.氢氧化钠溶液 D.乙醇
操作方法:E.蒸馏 F.分液 G.洗气 H.萃取
物质(括号中是杂质) | 除杂试剂 | 操作方法 |
①硝基苯(硝酸) | _____ | _____ |
②乙酸乙酯(乙酸) | _____ | _____ |
③甲烷(乙烯) | _____ | _____ |
(2)①乙酸中官能团的名称是__________________。
②工业上用乙烯水化法制备乙醇,反应的化学方程式是______________。
③红热的铜丝插入乙醇中反复几次发生反应,反应的化学方程式是______________,该反应类型为___________反应。
④丁烷有___________种同分异构体,其中___________(写名称)熔、沸点较低。
【题目】下列实验操作或事实与预期实验目的或所得结论对应正确的是
选项 | 实验操作或事实 | 实验目的或结论 |
A | 淡黄色试液 | 说明原溶液中一定含有Fe3+ |
B | 向AgNO3溶液中滴加过量氨水,溶液澄清 | Ag+与NH3H2O能大量共存 |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝 | NH4HCO3显碱性 |
D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于二元酸 |
A. A B. B C. C D. D
【题目】相同温度下,容积相同的3个恒温密闭容器中发生可逆反应:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.6KJ·mol-1
2NH3(g) ΔH=-92.6KJ·mol-1
实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始各物质的物质的量/mol | 达平衡时体系能量的变化 | |||
N2 | H2 | NH3 | Ar | ||
① | 1 | 3 | 0 | 0 | 放出热量:Q1 |
② | 0.9 | 2.7 | 0.2 | 0 | 放出热量:Q2 |
③ | 0.9 | 2.7 | 0.2 | 0.1 | 放出热量:Q3 |
下列比较正确的是
A. 放出热量大小:Q1>Q2=Q3
B. 容器中的压强:③>①=②
C. N2的转化率:①<②<③
D. 平衡时NH3的体积分数:①=②<③