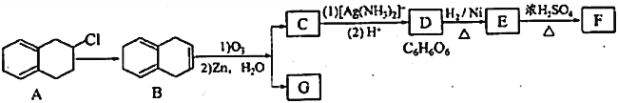
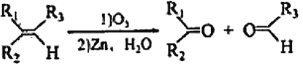题目内容
【题目】根据下图海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A. 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
B. 在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 在过程④、⑥反应中每氧化0.2molBr-需消耗2.24LCl2
D. 过程①的提纯是物理过程
【答案】A
【解析】
A.过程⑤中二氧化硫水溶液被氧化为硫酸:SO2+2H2O+Br2=2HBr+H2SO4,氢溴酸和硫酸都是强酸,对设备腐蚀严重,A项正确;
B.根据题给的信息 ,MgCl2·6H2O受热后会变成Mg(OH)Cl和HCl,进一步灼烧得到氧化镁,得不到无水氯化镁,B项错误;
C.没有指明氯气所处的温度和压强,气体摩尔体积体积Vm=22.4L/mol不能使用(如为标准状况则该说法正确),C项错误;
D.过程①除去可溶性杂质需要加入沉淀剂,是化学过程,D项错误;
所以答案选择A项。

练习册系列答案
相关题目