题目内容
【题目】某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图像判断错误的是( )

A. a值一定大于9
B. Ⅰ为NaOH溶液稀释时溶液的pH变化曲线
C. 完全中和稀释相同倍数后的两溶液,消耗相同浓度的稀H2SO4的体积V(NaOH)<V(氨水)
D. 稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
【答案】D
【解析】
氢氧化钠溶液和氨水具有相同的体积和pH,由于氢氧化钠是强电解质,则氢氧化钠的浓度小,氨水浓度大,在稀释时促进氨水的电离,则氨水中的离子浓度大,即I是氢氧化钠的pH变化曲线,Ⅱ是氨水的pH变化曲线,据此分析解答。
A.pH=11的氢氧化钠溶液加水稀释100倍,pH=9,而一水合氨为弱电解质,加水促进电离,则a的数值一定大于9,故A正确;
B.一水合氨为弱电解质,由图可知,开始的pH相同,在稀释时,促进氨水的电离,则氨水中的离子浓度大,可知I为氢氧化钠溶液稀释时溶液的pH变化曲线,Ⅱ是氨水的pH变化曲线,故B正确;
C.由于氨水浓度较大,则完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水),故C正确;
D.稀释后氨水中氢氧根离子浓度较大,则水的电离程度较小,故D错误;
故选D。

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案【题目】合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实现了人工固氮。
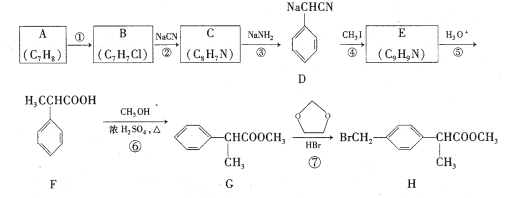
(1)反应N2(g)+3H2(g)![]() 2NH3(g)的化学平衡常数表达式为__。
2NH3(g)的化学平衡常数表达式为__。
(2)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是__。
序号 | 化学反应 | K(298K)的数值 |
① | N2(g)+O2(g) | 5×10-31 |
② | N2(g)+3H2(g) | 4.1×106 |
(3)某实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.100mol/L,c(H2)=0.300mol/L的反应物进行合成氨反应,N2的浓度随时间的变化如图①、②、③曲线所示。
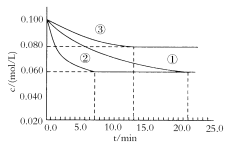
实验②平衡时H2的转化率为__。
据图所示,②、③两装置中各有一个条件与①不同。请指出,并说明判断的理由。
②条件:___理由:___。
③条件:___理由:___。