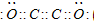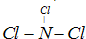题目内容
现有A、B、C、D、E、F六种短周期元素,原子序数依次增大.已知A与D、C与E分别同主族,D、E、F同周期.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C可形成电子总数相等的分子,且A与C,A与E,A与F也可以形成电子总数相等的分子.请回答下列问题:
(1)元素F在周期表中的位置______;
(2)A、C、D三种元素可组成一种常见化合物,该化合物的化学式______;工业生产该化合物和单质F的离子方程式为:______ Cl2↑+H2↑+2OH-
【答案】分析:A、B、C、D、E、F六种短周期元素,原子序数依次增大.A与D、C与E分别同主族,原子序数C大于A、B,小于E,所以C处于第二周期,E处于第三周期.D、E、F同周期,所以D、F也处于第三周期.
A分别与B、C可形成电子总数相等的分子,且A与C,A与E,A与F也可以形成电子总数相等的分子,元素A、B、C、F都为非金属,考虑10电子与18电子分子,A应为氢元素;D为钠元素;
与H元素形成10电子的元素有C、N、O、F元素,A、B的最外层电子数之和与C的最外层电子数相等,则B不可能为氟元素,若B为C元素,则C与E最外层电子数为5,则C为氮元素,E为磷元素,F为硫元素或氯元素,
H元素与N、P、S、Cl可以形成18电子分子,符合题意;
若B为N元素,则C与E最外层电子数为6,则C为氧元素,E为硫元素,F为氯元素,H元素与O、S、Cl可以形成18电子分子,符合题意;
结合问题(4)已知0.50mol EC2被C2氧化成气态EC3,可知B为C元素,C为氮元素,E为磷元素,F为硫元素或氯元素,不符合,
故B为N元素,C为氧元素,E为硫元素,F为氯元素,符合.
所以A应为氢元素;B为N元素,C为氧元素,D为钠元素;E为硫元素,F为氯元素.
解答:解:A、B、C、D、E、F六种短周期元素,原子序数依次增大.A与D、C与E分别同主族,原子序数C大于A、B,小于E,所以C处于第二周期,E处于第三周期.D、E、F同周期,所以D、F也处于第三周期.A分别与B、C可形成电子总数相等的分子,且A与C,A与E,A与F也可以形成电子总数相等的分子,元素A、B、C、F都为非金属,考虑10电子与18电子分子,A应为氢元素;D为钠元素;与H元素形成10电子的元素有C、N、O、F元素,A、B的最外层电子数之和与C的最外层电子数相等,则B不可能为氟元素,若B为C元素,则C与E最外层电子数为5,则C为氮元素,E为磷元素,F为硫元素或氯元素,H元素与N、P、S、Cl可以形成18电子分子,符合题意;若B为N元素,则C与E最外层电子数为6,则C为氧元素,E为硫元素,F为氯元素,H元素与O、S、Cl可以形成18电子分子,符合题意;结合问题(4)已知0.50mol EC2被C2氧化成气态EC3,可知B为C元素,C为氮元素,E为磷元素,F为硫元素或氯元素,不符合,故B为N元素,C为氧元素,E为硫元素,F为氯元素,符合.
所以A应为氢元素;B为N元素,C为氧元素,D为钠元素;E为硫元素,F为氯元素.
(1)F为氯元素,原子核外电子数为17,有3个电子层,最外层电子数为7,处于周期表第三周期VIIA族.
故答案为:第三周期VIIA族.
(2)A应为氢元素;C为氧元素,D为钠元素;三种元素可组成一种常见化合物,该化合物的化学式为NaOH;
工业上用电解饱和食盐水生成氢氧化钠与氯气,反应的离子方程式为2Cl-+2H2O Cl2↑+H2↑+2OH-.
Cl2↑+H2↑+2OH-.
故答案为:2Cl-+2H2O Cl2↑+H2↑+2OH-.
Cl2↑+H2↑+2OH-.
(3)B为N元素,F为氯元素,二者形成的化合物分子中,各原子最外层均达8电子结构,该分子为NCl3,分子中N原子与氯原子之间形成1对共用电子对,电子式为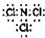 .
.
故答案为: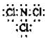 .
.
(4)已知0.50mol SO2被O2氧化成气态SO3,放出49.15kJ热量,则2molSO2反应放出的热量为49.15kJ×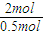 =196.6kJ,热化学方程式为 2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol;
=196.6kJ,热化学方程式为 2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol;
故答案为:2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol.
(5)A应为氢元素;B为N元素,C为氧元素,A、B、C以原子个数比4:2:3所形成的化合物,该化合物为NH4NO3,
铵根离子与硝酸根离子之间形成离子键,铵根离子中氮原子与氢原子之间形成共价键,硝酸根中碳原子与氧原子之间形成共价键;NH4NO3溶液中,铵根离子水解,溶液呈酸性,所以c(H+)>c(OH-),c(NO3-)>c(NH4+),水解程度很小,c(NH4+)远大于c(H+),所以离子浓度由大到小的顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-).
故答案为:c(NO3-)>c(NH4+)>c(H+)>c(OH-).
点评:本题是一个综合题,考查的知识点较多,能正确判断元素是解本题的关键,易错点是电子式的书写,注意不要漏写孤对电子.
A分别与B、C可形成电子总数相等的分子,且A与C,A与E,A与F也可以形成电子总数相等的分子,元素A、B、C、F都为非金属,考虑10电子与18电子分子,A应为氢元素;D为钠元素;
与H元素形成10电子的元素有C、N、O、F元素,A、B的最外层电子数之和与C的最外层电子数相等,则B不可能为氟元素,若B为C元素,则C与E最外层电子数为5,则C为氮元素,E为磷元素,F为硫元素或氯元素,
H元素与N、P、S、Cl可以形成18电子分子,符合题意;
若B为N元素,则C与E最外层电子数为6,则C为氧元素,E为硫元素,F为氯元素,H元素与O、S、Cl可以形成18电子分子,符合题意;
结合问题(4)已知0.50mol EC2被C2氧化成气态EC3,可知B为C元素,C为氮元素,E为磷元素,F为硫元素或氯元素,不符合,
故B为N元素,C为氧元素,E为硫元素,F为氯元素,符合.
所以A应为氢元素;B为N元素,C为氧元素,D为钠元素;E为硫元素,F为氯元素.
解答:解:A、B、C、D、E、F六种短周期元素,原子序数依次增大.A与D、C与E分别同主族,原子序数C大于A、B,小于E,所以C处于第二周期,E处于第三周期.D、E、F同周期,所以D、F也处于第三周期.A分别与B、C可形成电子总数相等的分子,且A与C,A与E,A与F也可以形成电子总数相等的分子,元素A、B、C、F都为非金属,考虑10电子与18电子分子,A应为氢元素;D为钠元素;与H元素形成10电子的元素有C、N、O、F元素,A、B的最外层电子数之和与C的最外层电子数相等,则B不可能为氟元素,若B为C元素,则C与E最外层电子数为5,则C为氮元素,E为磷元素,F为硫元素或氯元素,H元素与N、P、S、Cl可以形成18电子分子,符合题意;若B为N元素,则C与E最外层电子数为6,则C为氧元素,E为硫元素,F为氯元素,H元素与O、S、Cl可以形成18电子分子,符合题意;结合问题(4)已知0.50mol EC2被C2氧化成气态EC3,可知B为C元素,C为氮元素,E为磷元素,F为硫元素或氯元素,不符合,故B为N元素,C为氧元素,E为硫元素,F为氯元素,符合.
所以A应为氢元素;B为N元素,C为氧元素,D为钠元素;E为硫元素,F为氯元素.
(1)F为氯元素,原子核外电子数为17,有3个电子层,最外层电子数为7,处于周期表第三周期VIIA族.
故答案为:第三周期VIIA族.
(2)A应为氢元素;C为氧元素,D为钠元素;三种元素可组成一种常见化合物,该化合物的化学式为NaOH;
工业上用电解饱和食盐水生成氢氧化钠与氯气,反应的离子方程式为2Cl-+2H2O
 Cl2↑+H2↑+2OH-.
Cl2↑+H2↑+2OH-.故答案为:2Cl-+2H2O
 Cl2↑+H2↑+2OH-.
Cl2↑+H2↑+2OH-.(3)B为N元素,F为氯元素,二者形成的化合物分子中,各原子最外层均达8电子结构,该分子为NCl3,分子中N原子与氯原子之间形成1对共用电子对,电子式为
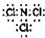 .
.故答案为:
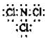 .
.(4)已知0.50mol SO2被O2氧化成气态SO3,放出49.15kJ热量,则2molSO2反应放出的热量为49.15kJ×
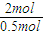 =196.6kJ,热化学方程式为 2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol;
=196.6kJ,热化学方程式为 2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol;故答案为:2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ/mol.
(5)A应为氢元素;B为N元素,C为氧元素,A、B、C以原子个数比4:2:3所形成的化合物,该化合物为NH4NO3,
铵根离子与硝酸根离子之间形成离子键,铵根离子中氮原子与氢原子之间形成共价键,硝酸根中碳原子与氧原子之间形成共价键;NH4NO3溶液中,铵根离子水解,溶液呈酸性,所以c(H+)>c(OH-),c(NO3-)>c(NH4+),水解程度很小,c(NH4+)远大于c(H+),所以离子浓度由大到小的顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-).
故答案为:c(NO3-)>c(NH4+)>c(H+)>c(OH-).
点评:本题是一个综合题,考查的知识点较多,能正确判断元素是解本题的关键,易错点是电子式的书写,注意不要漏写孤对电子.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.