题目内容
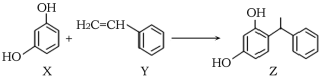
【题目】聚氨酯类高分子材料PU用途广泛,其合成反应为:
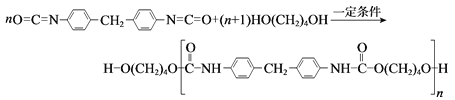
下列说法不正确的是( )
A. HO(CH2)4OH的沸点高于CH3CH2CH2CH3
B. 以1,3-丁二烯为原料,可合成HO(CH2)4OH
C. 合成PU的两种单体的核磁共振氢谱中均有3个吸收峰
D. 髙分子材料PU在强酸、强碱中均能稳定存在
【答案】D
【解析】
A. HO(CH2)4OH分子间可形成氢键,而CH3CH2CH2CH3不能,因此HO(CH2)4OH的沸点高于CH3CH2CH2CH3,A项正确;
B. 1,3-丁二烯和溴发生1,4加成反应,生成BrCH2-CH=CH-CH2Br,然后与氢气发生加成、再与氢氧化钠溶液发生取代反应生成HO(CH2)4OH,B项正确;
C. ![]() 以b线为中心对称,核磁共振氢谱有3个吸收峰,
以b线为中心对称,核磁共振氢谱有3个吸收峰, ![]() 中以a线为对称轴,核磁共振氢谱有3个吸收峰,C项正确;
中以a线为对称轴,核磁共振氢谱有3个吸收峰,C项正确;
D. 高分子材料PU含有酰胺键和酯基,在强酸、强碱中条件下均能发生水解,不能稳定存在,D项错误;
答案选D。

【题目】下列各项中I、II两个反应属于同一反应类型的是( )
选项 | 反应I | 反应II |
A |
| CH2=CH2→CH3CH2Cl |
B | CH3CH2Cl→CH3CH2OH | CH3CH2OH→CH3COOCH2CH3 |
C | CH3CH2OH→CH2=CH2 | CH3CH2OH→CH3CHO |
D | 油脂→甘油 |
|
A. AB. BC. CD. D
【题目】某学习小组用下列装置完成了探究浓硫酸和 SO2性质的实验(部分夹持装置已省略),下列“ 现象预测” 与“ 解释或结论” 均正确的是
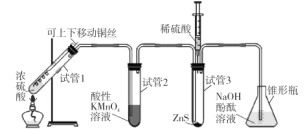
选项 | 仪器 | 现象预测 | 解释或结论 |
A | 试管1 | 有气泡、酸雾,溶液中有白色固体出现 | 酸雾是SO2所形成,白色固体是硫酸铜晶体 |
B | 试管2 | 紫红色溶液由深变浅,直至褪色 | SO2具有还原性 |
C | 试管3 | 注入稀硫酸后,没有现象 | 由于Ksp(ZnS)太小,SO2与ZnS在注入稀硫酸后仍不反应 |
D | 锥形瓶 | 溶液红色变浅 | NaOH溶液完全转化为NaHSO3溶液,NaHSO3溶液碱性小于NaOH |
A.AB.BC.CD.D