题目内容
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。请回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用____________形象化描述。在基态14C原子中,核外存在___________对自旋相反的电子。
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为__________________________。
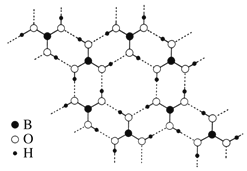
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
参数 分子 | 分子直径/nm | 分子与H2O的结合能E/kJ·mol-1 |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |

①下列关于CH4和CO2的说法正确的是________(填序号)。
a.CO2分子中含有2个σ键和2个π键
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0. 586 nm,根据上述图表所提供的数据分析,提出该设想的依据是______________________________________。
【答案】 电子云 2 H、C、O ad CO2的分子直径小于笼状空腔直径,且与H2O的结合力大于CH4
【解析】试题分析:本题考查电子云的概念、电负性的比较、σ键和π键的判断、杂化方式的判断、熔点高低的比较等。
(1)处于一定空间运动状态的电子在原子核外出现的概念密度分布可用电子云形象化描述。基态14C原子的轨道表示式为![]() ,核外存在2对自旋相反的电子。
,核外存在2对自旋相反的电子。
(2)CH4中C为-4价,H为+1价,电负性:C![]() H;非金属性:O
H;非金属性:O![]() C,电负性:O
C,电负性:O![]() C;C、H、O三种元素电负性由小到大的顺序为:H
C;C、H、O三种元素电负性由小到大的顺序为:H![]() C
C![]() O。
O。
(3)①a项,CO2的结构式为O=C=O,CO2分子中含有2个σ键和2个π键,a项正确;b项,CH4分子中含极性共价键,由于CH4为正四面体结构,CH4分子中正电中心和负电中心重合,CH4为非极性分子,b项错误;c项,CH4的相对分子质量小于CO2的相对分子质量,CH4分子间作用力小于CO2分子间作用力,CH4的熔点低于CO2,c项错误;d项,CH4中碳原子采取sp3杂化,CO2中碳原子采取sp杂化,d项正确;答案选ad。
②根据表中数据,CO2的分子直径(0.512nm)小于笼状结构的空腔直径(0.586nm),CO2与H2O的结合能(29.91kJ/mol)大于CH4与H2O的结合能(16.40kJ/mol),所以可用CO2置换“可燃冰”中的CH4。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:

苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生。请分别写出a仪器和c仪器的名称:_________________________、________________________________。
(2)请写出a中发生反应的化学方程式:___________________。d中倒置漏斗的作用是:_____,某同学认为如果想验证该反应的类型,可以取反应后烧杯d中溶液,加入稀硝酸酸化,然后加入硝酸银溶液,如果产生了淡黄色沉淀即验证了该反应的类型。试分析该同学的操作是否可行:______(填“是”或“否”),简要说明其原因:________________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
经以上分离操作后,粗溴苯中还含有的主要杂质为___,要进一步提纯,下列操作中必须的是____(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取