题目内容
16.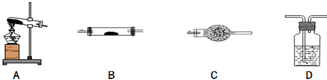 草酸亚铁晶体的化学式为FeC2O4•2H2O,它是一种淡黄色结晶粉末,有轻微刺激性,加热时可发生如下分解反应:FeC2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO2↑+CO↑+2H2O
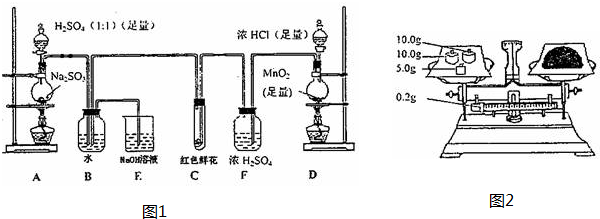
草酸亚铁晶体的化学式为FeC2O4•2H2O,它是一种淡黄色结晶粉末,有轻微刺激性,加热时可发生如下分解反应:FeC2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO2↑+CO↑+2H2O(1)请你用图中提供的仪器(可以重复选用,但每种仪器至少选用一次),选择必要的试剂[供选择的试剂:NaOH溶液、澄清石灰水、饱和碳酸钠溶液、CuO、无水硫酸铜、酸性高锰酸钾溶液],设计一个实验,检验FeC2O4•2H2O加热时分解产生的气态产物(包括水蒸气)(部分加热装置和夹持仪器在图中略去).在答题卡上填写表格(可以不用填满,也可以补充).
| 仪器符号 | 仪器中所加物质 | 作用 |
| A | 草酸亚铁晶体 | 加热草酸亚铁晶体得到气体产物 |
| D | NaOH溶液 | |
(3)反应结束后,在A装置试管中有黑色固体粉末(混合物)产生,倒出时存在燃烧现象,产生上述现象的可能原因是FeC2O4•2H2O分解产生的CO将部分FeO还原为粉末状的单质铁,铁粉被空气中的氧气氧化而燃烧.
分析 (1)FeC2O4•2H2O加热时分解产生的气态产物有水蒸气、CO2、CO,检验产生的气态产物时,可以先用无水硫酸铜检验水,然后通过澄清石灰水检验二氧化碳,再用氢氧化钠溶液除去二氧化碳,再通过灼热的氧化铜,将生成的气体再通过澄清石灰水,检验CO与氧化铜反应生成的二氧化碳,据此答题;
(2)照题目提供的装置和要求设计的实验没有尾气吸收装置,而一氧化碳有毒,会污染空气;
(3)在A装置试管中有黑色固体粉末有可能是被还原出来的铁粉,铁粉被空气中的氧气氧化而燃烧,据此答题;
解答 解:(1)FeC2O4•2H2O加热时分解产生的气态产物有水蒸气、CO2、CO,检验产生的气态产物时,可以先用无水硫酸铜检验水,然后通过澄清石灰水检验二氧化碳,再用氢氧化钠溶液除去二氧化碳,再通过灼热的氧化铜,将生成的气体再通过澄清石灰水,检验CO与氧化铜反应生成的二氧化碳,所以设计的实验为
| 仪器符号 | 仪器中所加物质 | 作用 |
| A | 草酸亚铁晶体 | 加热草酸亚铁晶体得到气体产物 |
| C | 无水硫酸铜 | 检验H2O |
| D | 澄清石灰水 | 检验CO2 |
| D | NaOH溶液 | 除去未反应的CO2 |
| D | 澄清石灰水(无此步不扣分) | 检验CO2是否已除尽 |
| B | CuO | CO与CuO反应生成CO2 |
| D | 澄清石灰水 | 检验CO与CuO反应生成的CO2 |
故答案为:
| 仪器符号 | 仪器中所加物质 | 作用 |
| A | 草酸亚铁晶体 | 加热草酸亚铁晶体得到气体产物 |
| C | 无水硫酸铜 | 检验H2O |
| D | 澄清石灰水 | 检验CO2 |
| 除去未反应的CO2 | ||
| D | 澄清石灰水(无此步不扣分) | 检验CO2是否已除尽 |
| B | CuO | CO与CuO反应生成CO2 |
| D | 澄清石灰水 | 检验CO与CuO反应生成的CO2 |
(2)按照题目提供的装置和要求设计的实验没有尾气吸收装置,而一氧化碳有毒,会污染空气,
故答案为:未对尾气进行处理,可造成环境污染;
(3)因为FeC2O4•2H2O分解产生的CO将部分FeO还原为粉末状的单质铁,所以在A装置试管中有黑色固体粉末有可能是被还原出来的铁粉,铁粉被空气中的氧气氧化而燃烧,
故答案为:FeC2O4•2H2O分解产生的CO将部分FeO还原为粉末状的单质铁,铁粉被空气中的氧气氧化而燃烧.
点评 本题考查了铁及其化合物性质的实验验证和实验设计,灵活运用实验基本操作是解题关键,题目难度较大.

练习册系列答案
相关题目
7.下列有关化学键的叙述,正确的是( )
| A. | 非金属元素组成的化合物中只含共价键 | |
| B. | 水溶液能导电的化合物一定是离子化合物 | |
| C. | 化合物MgO、SiO2、SO3中化学键的类型相同 | |
| D. | PH3分子稳定性低于NH3分子,因为N-H键键能高 |
4.室温下,下列溶液中粒子浓度关系正确的是( )
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O${\;}_{4}^{-}$)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO${\;}_{3}^{2-}$)+c(OH-) | |
| D. | CH3COONa溶液:c(Na+)>c(CH3COO-) |
1.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如图(废料中含有Al、Li、Co2O3和Fe2O3等物质).
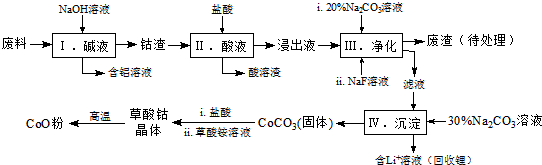
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表.
请回答:
(1)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(2)步骤Ⅲ中 Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过;废渣中的主要成分除了LiF外,还有Fe(OH)3.
(3)NaF 与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(4)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表.已知:M(CoC2O4•2H2O)=183g/mol
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是3CoC2O4+2O2 $\frac{\underline{\;210℃-290℃\;}}{\;}$Co3O4+6CO2.温度高于890℃时,固体产物发生分解反应,固体产物为CoO.

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表.
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(2)步骤Ⅲ中 Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过;废渣中的主要成分除了LiF外,还有Fe(OH)3.
(3)NaF 与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(4)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表.已知:M(CoC2O4•2H2O)=183g/mol
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
8.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③沸点:H2Se>H2S>H2O④结合H+能力:OH->CH3COO->I-.
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③沸点:H2Se>H2S>H2O④结合H+能力:OH->CH3COO->I-.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
5.下列反应的离子方程式中正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| B. | 氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 碳酸钙溶于稀醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |