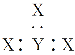题目内容
【题目】镓是一种低熔点高沸点的稀有金属,有“电子工业脊梁”的美誉,被广泛应用到光电子工业和微波通信工业;镓(Ga)与铝位于同一主族,金属镓的熔点是29.8℃,沸点是2403℃。
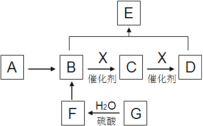
(1)工业上利用Ga(l)与NH3(g)在1000℃高温下合成半导体固体材料氮化镓(GaN),同时生成氢气,每生成lmol H2时放出10.3 kJ热量。写出该反应的热化学方程式__________________。
(2)在密闭容器中,充入一定量的Ga与NH3发生反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。
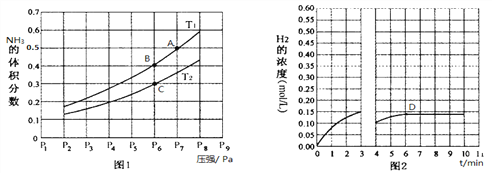
① 图1中A点和C点化学平衡常数的大小关系是:KA_____KC,(填“<”、“=”或“>”),理由是__________________________________________________。
② 该反应在T1和P6条件下至3min时达到平衡,此时改变条件并于D点处重新达到平衡,H2的浓度随反应时间的变化趋势如图2所示(3~4 min的浓度变化未表示出来),则改变的条件为__________(仅改变温度或压强中的一种)。
(3)若用压强平衡常数Kp表示,此时B点对应的Kp=__________(用含P6的式子表示)(Kp为压强平衡常数,用平衡分压代替平衡浓度计算,气体平衡分压=总压×气体体积分数)
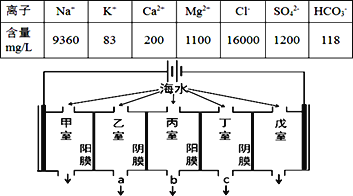
(4)电解精炼法提纯镓的具体原理如下:以粗镓(含Zn、Fe、Cu杂质)为阳极,以高纯镓为阴极,以NaOH溶液为电解质。在电流作用下使粗镓溶解进入电解质溶液,并通过某种离子迁移技术到达阴极并在阴极放电析出高纯镓。
①已知离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+。电解精炼镓时阳极泥的成分是_________。
②阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,写出GaO2-在阴极放电的电极反应式是_____________。
【答案】 2Ga(l)+2NH3(g)=2GaN(s)+3H2(g) ΔH=-30.9 kJ·mol-1 < 由第1问可知该反应为放热反应,其他条件一定时,温度升高, 平衡逆向移动,此时NH3的体积分数越大而K值减小 减小压强 ![]() Fe、Cu GaO2- + 3e- + 2H2O = Ga+4OH-
Fe、Cu GaO2- + 3e- + 2H2O = Ga+4OH-
【解析】(1)反应的方程式为2Ga(s)+2NH3(g)2GaN(s)+3H2(g),生成3mol H2时放出30.9kJ的热量,可知热化学方程式为2Ga(s)+2NH3(g)2GaN(s)+3H2(g)△H=-30.9kJ/mol,故答案为:2Ga(s)+2NH3(g)2GaN(s)+3H2(g)△H=-30.9kJ/mol;
(2)①2Ga(s)+2NH3(g)2GaN(s)+3H2(g)△H=-30.9kJ/mol,为放热反应,对于放热反应而言,温度升高,平衡逆向移动,K减小,A点平衡常数小于C点平衡常数,故答案为:<;对于放热反应而言,其他条件一定时,温度升高, 平衡逆向移动,此时NH3的体积分数越大而K值减小;
②结合图示,改变的外界条件是降低压强,气体的体积增大,氢气的浓度减小,平衡向气体体积增大的方向进行,随后,氢气的浓度又逐渐增大,但会小于原平衡的浓度,故答案为:减小压强;
(3)2Ga(s)+2NH3(g)2GaN(s)+3H2(g),用某组份(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作Kp),且PB=P×B的体积分数。则该反应的化学平衡常数表达式(Kp)=![]() =
=![]() ,故答案为:
,故答案为:![]() ;
;
(4)①离子氧化性顺序为:Zn2+<Ga3+<Fe2+<Cu2+,则金属还原性顺序为Zn>Ge>Fe>Cu,则阳极上Zn、Ge失电子进入电解质溶液,Fe、Cu以金属单质形成阳极泥,则阳极泥成分是Fe、Cu,故答案为:Fe和Cu;
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,该反应的离子方程式为Ga3++4OH-=GaO2-+2H2O;阴极上GaO2-得电子发生还原反应生成Ga,电极反应式为GaO2-+3e-+2H2O=Ga+4OH-;故答案为:GaO2-+3e-+2H2O=Ga+4OH-。

【题目】—氯甲烷是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
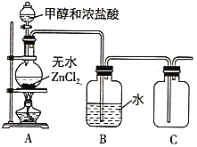
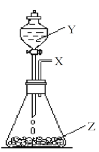
(1)某小组同学在实验室用如图所示装置模拟催化法制备和收集一氯甲烷。
①装置B的主要作用是_____。
②以无水ZnCl2为催化剂,圆底烧瓶中发生反应的化学方程式为____。如果实验时圆底烧瓶加热时间过长,最终在瓶底得到一种白色物质,该物质的化学式是____。
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mLc1mol/LNaOH溶液充分吸收,以甲基橙作指示剂,用c2mol/L盐酸标准液对吸收液进行滴定,最终消耗V2mL盐酸,则所收集CH3Cl的物质的量为_____mol。(已知:2CH3Cl+3O2=2CO2+2H2O+2HCl)
(2)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子。相关数据如下表:
化学键 | C-Cl | C-Br |
键能/(kJ·mol-1) | 330 | 276 |
化合物 | AgCl | AgBr |
Ksp | 1.8×10-10 | 5×10-13 |
①CH3X通入AgNO3的乙醇溶液中,除有沉淀生成外,还生成硝酸甲酯,请写出硝酸甲酯的结构简式:_____。
②设计实验证明HBr是强酸:____(简要说明实验操作、现象和结论)
③CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀。请依据表中的键能和Ksp数据解释原因:____。