题目内容
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A.红棕色的NO2 , 加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.Fe(SCN)3溶液中加入固体KSCN后颜色变深
D.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
【答案】D
【解析】A.可逆反应2NO2 ![]() N2O4 , 加压条件下,体积减小,混合气体各组分的浓度增大,故颜色变深,但增大压强,平衡向气体体积减小的方向移动,即正向移动,颜色逐渐变浅,所以可以用平衡移动原理解释,A项不符合题意;
N2O4 , 加压条件下,体积减小,混合气体各组分的浓度增大,故颜色变深,但增大压强,平衡向气体体积减小的方向移动,即正向移动,颜色逐渐变浅,所以可以用平衡移动原理解释,A项不符合题意;
B.2SO2+O2(g) ![]() 2SO3(g),正反应为气体体积减小的反应,增大压强,平衡向正反应移动,有利于合成SO3 , 能用平衡移动原理解释,B项不符合题意;
2SO3(g),正反应为气体体积减小的反应,增大压强,平衡向正反应移动,有利于合成SO3 , 能用平衡移动原理解释,B项不符合题意;
C.向硫氰化铁溶液中加入硫氰化钾固体时,硫氰根离子浓度增大,平衡向正反应方向移动,则硫氰化铁浓度增大,溶液的颜色变深,可用平衡移动原理解释,C项不符合题意;
D.H2+I2(g) ![]() 2HI(g),该反应前后气体的体积不变,增大压强,平衡不移动,增大平衡体系的压强气体的体积减小,碘的浓度增大,颜色变深,不能用平衡移动原理解释,D项符合题意。勒夏特列原理(又称平衡移动原理)主要内容为:在一个已经达到平衡的反应中,如果改变ing想平衡的条件之一(如温度、压强,以及参加化学反应的物质的浓度),平衡将向着减弱这种改变的方向移动。
2HI(g),该反应前后气体的体积不变,增大压强,平衡不移动,增大平衡体系的压强气体的体积减小,碘的浓度增大,颜色变深,不能用平衡移动原理解释,D项符合题意。勒夏特列原理(又称平衡移动原理)主要内容为:在一个已经达到平衡的反应中,如果改变ing想平衡的条件之一(如温度、压强,以及参加化学反应的物质的浓度),平衡将向着减弱这种改变的方向移动。
A、2NO2 N2O4,加压使浓度瞬间增大,颜色加深,据移动原理,平衡向压强减小方向进行 , 颜色变浅
B、2SO2+O2(g) 2SO3(g),增大压强,平衡向压强减小方向进行,有利于合成SO3
C、Fe3++3SCN-=Fe(SCN)3加入固体KSCN,使SCN-浓度增大,平衡向减小SCN-浓度的方向移动
D、H2+I2(g) 2HI(g),反应前后气体压强不变,所以加压,平衡不移动。但加压造成各物质浓度增大,气体颜色加深。

【题目】四种短周期元素在周期表中的位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.请回答下列问题:
X | Y | |
Z | W |
(1)元素Z位于周期表中第_____周期,_____族;
(2)比较X与Y的气态氢化物的稳定性:_____(写化学式);
(3)XW2的电子式为_____;
(4)比较X、Y、Z、W四种原子半径由大到小关系:_____;
(5)X和W形成的化合物属于_____ (填“离子化合物”、或“共价化合物”),该化合物中存在的微粒间作用力有:_____.
【题目】NO2为红棕色气体,可在火箭燃料中作氧化剂。回答下列问题:
(1)火箭用N2H4和NO2作燃料,产物绿色无污染,该反应的化学方程式为____________。
(2)为探究NO2和铁粉反应的产物,某小组按下图所示装置进行实验。
已知:①二者反应可能的还原产物为N2或NO
②沸点:NO2(21℃),NO(-152℃)
③酸性KMnO4溶液能氧化NO生成NO3-
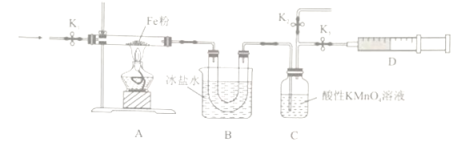
①按上图所示组装完实验仪器后,下一步操作为______________________________。
②实验前需利用气体X将装置的空气排净,气体X可以为_______(填标号)。
A.Ar B.H2 C.CO D.NO2
③排净空气后,后续实验的最佳操作顺序是___c、b(填标号)。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.打开K1和K2,关闭K3,缓缓通入气体X
d.打开K1和K3,关闭K2,缓缓通入NO2 e.关闭K1,停止通入NO2
④装置B的作用是__________________________________。
(3)分析NO2和铁粉反应的产物
①实验过程中A、C装置的物质均无明显颜色变化,D收集到无色气体。由此可推知气体产物为____________________________。
②取少量固体产物于试管,先加入盐酸充分溶解,再加入KSCN溶液,溶液若无血红色,则产物不含三价铁。该方案是否可行并说明理由:_______________________________。
③实验得到的相关数据如下表:
玻璃管质量/g | Fe质量/g | 反应后(玻璃管+固体)/g |
m | 1.12 | m+1.52 |
综合实验现象和计算可知,固体生成物一定有______(填“FeO”Fe2O3”或“Fe3O4”);反应的方程式为______
