题目内容
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元
素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是( )
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
D
解析试题分析:根据题意可知:W是Na;X是O;Z是S;Y是Cl. A.Y元素最高价氧化物对应的水化物化学式HYO4。错误。B.Na、S、Cl是同一周期的元素.对于电子层数相同的元素来说,原子序数越大,原子半径就越小。所以原子半径由大到小的顺序为:W >Z>Y 。错误。D.Na和O可以形成Na2O和Na2O2两种化合物,阴、阳离子物质的量之比均为1:2。正确。
考点:考查元素周期表、元素周期律及元素和化合物的知识。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
下列有关元素的性质及其递变规律正确的是( )
| A.IA族与ⅦA族元素间形成的化合物都是离子化合物 |
| B.第三周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,其单质的氧化性越强 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X所处的周期序数与族序数相等。下列说法错误的是( )
| A.Z的氧化物与W的氧化物的化学键类型相同 |
| B.X、Z的氧化物都能溶于氢氧化钠和稀硫酸溶液中 |
| C.最高价氧化物对应水化物稀溶液的氧化性:W<Z |
| D.Y原子的半径比W原子的半径大 |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族;X+与M2—具有相同的电子层结构;离子半径:Z2—>W—;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
| A.X、M两种元素只能形成X2M型化合物 |
| B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| C.元素Y、Z、W的单质晶体属于同种类型的晶体 |
| D.元素W和M的某些单质可作为水处理中的消毒剂 |
下列说法正确的是( )
| A.IA族元素的金属性比ⅡA族元素的金属性强 |
| B.Ⅵ族元索的氢化物中,稳定性最好的其沸点也最高 |
| C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强 |
| D.第三周期元素的离子半径从左到右逐渐减小 |
某微粒用符号ZAMn+表示,下列关于该微粒的叙述正确的是
| A.所含质子数为(A-n) | B.所含中子数为(A-Z) |
| C.所含电子数为(Z+n) | D.中子数-电子数=A-2Z-n |
某原子核内的质子数为m,中子数为n,则下述论断正确的是( )
| A.原子核内中子的总质量小于质子的总质量 |
| B.该原子的质量数等于m-n |
| C.该元素的相对原子质量近似等于m+n |
| D.该原子的相对原子质量近似等于m+n |
几种短周期元素的原子半径及某些化合价见下表,下列说法正确的是( )
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | –1 | –2 | +4、–4 | +7、–1 | +5、–3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
B.A、H、J的离子半径由大到小顺序是A>J>H
C.G元素的单质不存在同素异形体
D.I在DB2中燃烧生成两种化合物
下表为周期表的一部分,有关短周期X、Y、Z、R四种元素叙述正确的是: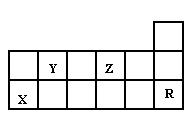
| A.热稳定性:Y的气态氢化物<Z的气态氢化物 |
| B.X的最高价氧化物对应水化物的酸性比Y的强 |
| C.X元素的单质能与所有强酸发生反应放出H2 |
| D.R元素的单质化学性质活泼 |