题目内容
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
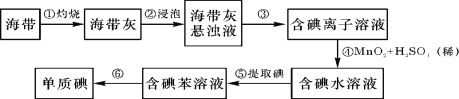
(1)从上述步骤中可知,海带中含有的碘元素的主要存在形式是 (填化学式)。
(2)步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A烧杯 B表面皿 C坩埚 D酒精灯 E干燥器
(3)步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指列实验装置中的错误之处。
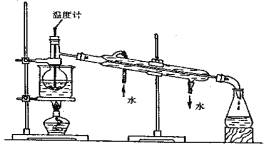
① ;② ;③ ;
进行上述蒸馏操作时,使用水浴的原因是 ;最后晶态碘在 里聚集。
(4)步骤④反应的离子方程式是 。若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I—,写出反应的离子方程式 。
(5)检验海带中是否含有碘元素,可以在步骤④后进行,检验时可用的试剂是 。
(6)步骤⑤中,某学生选择用苯来提取碘,其实验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈中;
(B)把50毫升碘水和15毫升苯加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗活塞和上口的玻璃塞是否漏液;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接收溶液;
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。
就此实验,完成下列填空:
正确操作步骤的顺序是 → → →A→G→ →E→F
【答案】(1)I—;
(2)C D;
(3)①温度计水银球位置没有放在蒸馏烧瓶的支管口;②冷凝管中的水流方向错误;③加热时在烧杯上没有垫石棉网;使用水浴的原因:受热均匀,容易控制反应温度, 反应温度低于100℃;蒸馏烧瓶;
(4)2I—+4H++MnO2=I2+Mn2++2H2O;5I—+6H++IO3-=3I2+3 H2O
(5)淀粉;
(6)C;B;D;H。
【解析】
试题分析:(1)步骤③得到含碘离子的溶液,故答案为:碘离子;
(2)灼烧固体物质一般使用(瓷)坩埚,而坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,故答案为:CD;
(3)根据蒸馏的注意事项可知,图中出现以下错误:①温度计水银球的位置错误,应与蒸馏瓶支管下沿平齐;②烧杯下没垫石棉网,否则加热时会受热不均而炸裂;③冷冷凝管中凝水的流向错误,冷水应从下方进,上方出;用酒精灯直接加热温度变化快,而水浴加热试管内试剂受热比较均匀;步骤⑥是从含碘苯溶液中分离出单质碘和回收苯;所以碘在蒸馏烧瓶中聚集;故答案为:①温度计水银球的位置错误,应与蒸馏瓶支管下沿平齐;②烧杯下没垫石棉网,否则加热时会受热不均而炸裂;③冷冷凝管中凝水的流向错误,冷水应从下方进,上方出;受热均匀,容易控制反应温度, 反应温度低于100℃;蒸馏烧瓶;
(4)碘离子在酸性条件下可被MnO2氧化,反应的离子方程式为2I-+MnO2+4H+=Mn2++I2+2H2O;若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I—生成碘单质,反应的离子方程式为5I—+6H++IO3-=3I2+3 H2O,故答案为:2I-+MnO2+4H+=Mn2++I2+2H2O;5I—+6H++IO3-=3I2+3 H2O;
(5)碘遇淀粉变蓝色,故答案为:淀粉试液;
(6)CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,操作为查漏→装液→振荡→静置→分液,则步骤为C→B→D→A→G→H→E→F,故答案为:C;B;D;H。

 阶梯计算系列答案
阶梯计算系列答案