题目内容
【题目】如图是M、N两种主族元素的原子结构示意图,下列说法正确的是( )
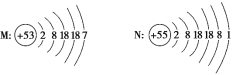
A.M位于第五周期Ⅶ族
B.N位于IA族,该主族中的元素又称为碱金属元素
C.N在空气中燃烧,生成化学式为N2O的氧化物
D.M所在的主族中各元素是同周期元素中非金属性最强的元素
【答案】D
【解析】
A.M原子有5个电子层,最外层有7个电子,故M位于第5周期第ⅦA族,M是I,故A错误;
B.N原子有6个电子层,最外层有1个电子,故N位于第6周期第ⅠA族,N是Cs,该主族中除了H以外的所有元素又称为碱金属元素,故B错误;
C.根据原子结构示意图,N为Cs,碱金属大多数金属性很强,在空气中燃烧产物较复杂,只有Li在空气中燃烧生成氧化物,其它的在空气中燃烧生成过氧化物或超氧化物,故C错误;
D.M位于第5周期第ⅦA族,同周期元素从左到右元素的非金属性逐渐增强,M所在的主族各元素是同周期元素中非金属性最强的元素,故D正确;
答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】硫代硫酸钠(Na2S2O3)可用作分析试剂、基准试剂、还原剂、除氯剂等。
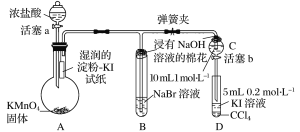
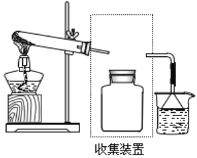
Ⅰ、实验室制备硫代硫酸钠装置图如下。

(1)仪器B的名称是________。
(2)写出装置B制备Na2S2O3的化学反应方程式____________________________。
(3)NaOH溶液的作用是____________________________________。
Ⅱ、测硫代硫酸钠样品纯度步骤如下
①称取Ⅰ中制得硫代硫酸钠样品8.0g配成250mL溶液
②从①中量取20.00mL溶液于锥形瓶中
③用0.lmol·L-1标准碘液滴定,实验测得数据如下
滴定前读数(mL) | 滴定后读数(mL) | 待测液体积(mL) | |
实验一 | 1.20 | 21.00 | 20.00 |
实验二 | 0.40 | 19.20 | 20.00 |
实验三 | 0.50 | x | 20.00 |
(4)该滴定时,向锥形瓶中加入1至2滴淀粉液作指示剂,则达到滴定终点的判断标准是______________。
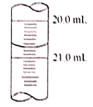
(5)x读数如图所示,则x=________,根据所测的数据计算该硫代硫酸钠样品纯度为_______________。(已知I2+2Na2S2O3=2NaI+Na2S4O6)
(6)若步骤①中量取20.00mL硫代硫酸钠溶液时,未用硫代硫酸钠溶液润洗滴定管,则测得样品的纯度将______________(填“偏大”或“偏小”)。