题目内容
【题目】某化学课外兴趣小组为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
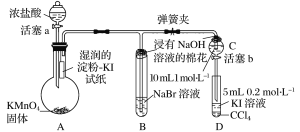
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ. ……
(1)盛放浓盐酸的仪器名称为____________________。
(2)在烧瓶内发生反应时,体现浓盐酸的性质为__________________。
(3)验证氯气的氧化性强于碘的实验现象是__________________________。
(4)B中溶液发生反应的离子方程式是____________________________。
(5)浸有NaOH溶液的棉花的作用为______________________________。
(6)为验证溴的氧化性强于碘,过程Ⅳ的操作步骤和现象是______________。
(7)过程Ⅲ实验的目的是________________________________。
【答案】分液漏斗 还原性和酸性 湿润的淀粉KI试纸变蓝 Cl2+2Br-=Br2+2Cl- 吸收挥发出来的Cl2,防止污染空气 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后CCl4层变为紫红色 确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰
【解析】
装置A:高锰酸钾溶液和浓盐酸反应生成氯化锰、氯化钾、氯气和水,装置A中生成氯气,烧瓶上端湿润的碘化钾淀粉试纸变蓝色,验证氯气的氧化性强于碘;装置B:装置B中盛有溴化钠,氯气进入装置B中,氯气氧化溴离子为溴单质,溶液呈橙红色,验证氯的氧化性强于溴,氯气有毒,能被氢氧化钠吸收,浸有氢氧化钠的棉花防止氯气污染空气;当B和C中的溶液都变为黄色时,夹紧弹簧夹,为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论。
(1)根据装置图可知盛放浓盐酸的仪器名称为分液漏斗;
(2)在烧瓶内发生反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,在该反应中Cl元素的化合价由反应前HCl中的-1价变为反应后Cl2中的0价,化合价升高,失去电子,HCl表现还原性,作还原剂;还有一部分Cl元素化合价反应前后没有发生变化,与反应产生的金属阳离子结合形成盐,起酸的作用,所以该反应中浓盐酸体现了还原性和酸性;
(3)在A上部的湿润kI淀粉试纸上发生反应:Cl2+2I-=I2+2Cl-,I2能使淀粉变蓝,根据氧化剂的氧化性大于氧化产物的氧化性,可知Cl2的氧化性大于I2的氧化性,反应现象是湿润的淀粉KI试纸变蓝;
(4)因Cl2的氧化性大于Br2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,可发生:Cl2+2Br-=Br2+2Cl-;
(5)氯气有毒,能被氢氧化钠吸收,浸有氢氧化钠的棉花的作用是吸收挥发出来的Cl2,防止氯气污染空气;
(6)因Br2的氧化性大于I2的氧化性,根据氧化剂的氧化性大于氧化产物的氧化性,要发生:Br2+2I-=I2+2Br-,过程IV的操作和现象是打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡,静置后CCl4层溶液变为紫红色;
(7)为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论,过程III实验的目的是确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰。

 阅读快车系列答案
阅读快车系列答案