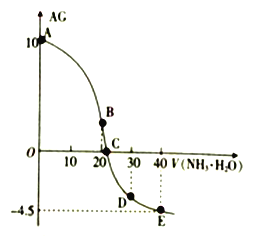
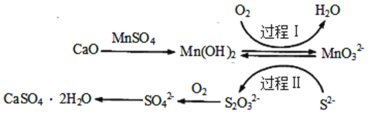
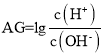题目内容
【题目】工业上常采用“电催化氧化—化学沉淀法”对化学镀镍废水进行处理,电解过程中电解槽中H2O、Cl-放电产生·OH、HClO,在活性组分作用下,阴阳两极区发生的反应如下(R表示有机物):
①R+·OH→CO2+H2O
②R+HClO→CO2+H2O+Cl-
③H2PO![]() +2·OH-4e-=PO
+2·OH-4e-=PO![]() +4H+
+4H+
④HPO![]() +·OH-2e-=PO
+·OH-2e-=PO![]() +2H+
+2H+
⑤H2PO![]() +2ClO-=PO
+2ClO-=PO![]() +2H++2Cl-
+2H++2Cl-
⑥HPO![]() +ClO-=PO
+ClO-=PO![]() +H++Cl-
+H++Cl-
⑦Ni2++2e-=Ni
⑧2H++2e-=H2↑
下列说法不正确的是( )
A.·OH、HClO在阳极上产生
B.增大电极电压,电化学氧化速率加快
C.电解时,阴极附近pH逐渐升高,Ni2+去除率逐渐减小
D.向电解后的废水中加入CaCl2可以去除磷元素
【答案】C
【解析】
A. 电解过程中电解槽中H2O、Cl-放电产生·OH、HClO,可得电极反应为:![]() ,
,![]() ,失电子在阳极反应,故A正确;
,失电子在阳极反应,故A正确;
B. 增大电极电压,可以加快导线中电子的移动速度,同时加快溶液中离子的移动速度,提高电化学氧化速率加快,故B正确;
C. 电解时,阴极反应为Ni2++2e-=Ni,2H++2e-=H2↑,镍离子得电子转变成金属单质除去,pH升高后,镍离子能与氢氧根结合成氢氧化镍沉淀,仍然可以从废水中去除,因此没有降低其去除效率,故C错误;
D. 向电解后的废水中加入CaCl2可以与产生的磷酸根离子形成磷酸钙沉淀,从而去除废水中的磷元素,故D正确;
故选:C。

练习册系列答案
相关题目