题目内容
【题目】常温下,用![]() 溶液分别滴定
溶液分别滴定![]() 的
的![]() 溶液和
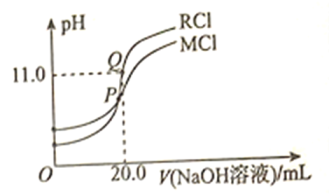
溶液和![]() 溶液,滴定曲线如图所示,下列说法错误的是( )
溶液,滴定曲线如图所示,下列说法错误的是( )
A.同条件下的碱性:![]()
B.![]()
C.![]()
D.P点时![]() 溶液中存在
溶液中存在![]()
【答案】C
【解析】
A.由图像可知相同物质的量浓度的![]() 溶液和MCl溶液,MCl溶液的pH大于RCl溶液的pH,说明RCl的水解程度大,根据盐类水解规律-越弱越水解可知MCl对应碱的碱性强于RCl对应碱的碱性,即
溶液和MCl溶液,MCl溶液的pH大于RCl溶液的pH,说明RCl的水解程度大,根据盐类水解规律-越弱越水解可知MCl对应碱的碱性强于RCl对应碱的碱性,即![]() ,故A正确;
,故A正确;
B.当氢氧化钠体积为20mL时恰好与![]() 完全反应产生ROH,溶液中存在:
完全反应产生ROH,溶液中存在:![]() ,c(ROH)=
,c(ROH)=![]() ,
,![]() ,
,![]() ,
,![]() ,故B正确;
,故B正确;
C.由题意可知,氢氧化钠的浓度与盐溶液的浓度相同,因此加入与盐溶液等体积的氢氧化钠时反应达到终点,结合图像可知MCl溶液的滴定终点在氢氧化钠体积20.0mL之前,说明MCl溶液![]() ,故C错误;
,故C错误;
D. P点为![]() 溶液的滴定终点,此时
溶液的滴定终点,此时![]() 恰好与氢氧化钠完全反应产生MOH和NaCl,因氯化钠为强酸强碱盐只电离不水解,电离产生等量的钠离子和氯离子,因此溶液中的
恰好与氢氧化钠完全反应产生MOH和NaCl,因氯化钠为强酸强碱盐只电离不水解,电离产生等量的钠离子和氯离子,因此溶液中的![]() ,故D正确;
,故D正确;
故选:C。

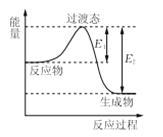
【题目】化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。
(1)键能也可以用于估算化学反应的反应热(ΔH)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ·mol-1) | 172 | 335 | 498 | X |
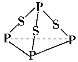
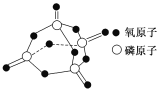
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图所示,则上表中X=________。
(2)1840年,俄国化学家盖斯在分析了许多化学反应热效应的基础上,总结出一条规律:“一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的.”这个规律被称为盖斯定律.有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。
①已知:
C(石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ/mol①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ/mol②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599.2 kJ/mol③
则由C(石墨)和H2(g)反应生成1 mol C2H2(g)的焓变为__________________。
②已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出x kJ热量。已知单质碳的燃烧热为y kJ/mol,则1 mol C与O2反应生成CO的反应热ΔH为______________。