题目内容
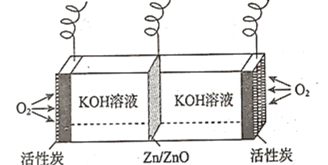
【题目】锌空气燃料电池广泛用于铁路、航海灯标以及助听器中,其装置示意图如图所示。下列说法错误的是( )
A.放电时,负极的电极反应式为![]()
B.放电时,![]() 向活性炭电极方向移动
向活性炭电极方向移动
C.充电时,![]() 电极上的电势比活性炭电极上的高
电极上的电势比活性炭电极上的高
D.充电时阴极质量减小![]() ,理论上阳极生成
,理论上阳极生成![]() 气体
气体
【答案】C
【解析】
根据电极材料可知,放电时Zn/ZnO电极为负极,通入氧气的活性炭电极为正极,则充电时Zn/ZnO电极为阴极,通入氧气的活性炭电极为阳极。
A.放电时Zn/ZnO电极为负极,Zn失电子结合OHˉ转化为ZnO,电极反应式为![]() ,故A正确;
,故A正确;
B.原电池中阳离子流向正极,所以K+向活性炭电极方向移动,故B正确;
C.充电时,Zn/ZnO电极与外加电源负极相连,为阴极,活性炭与外加电源正极相连,为阳极,阴极电势要低于阳极,即Zn/ZnO电极上的电势比活性炭电极上的低,故C错误;
D.充电时阴极上ZnO转化为Zn,电极反应式为ZnO+2eˉ+H2O=Zn+2OHˉ,所以减少的质量为O原子的质量,质量减少16g,即减少1mol氧原子,转移2mol电子,阳极生成的气体为氧气,生成一个氧气转移4个电子,所以转移2mol电子时生成0.5mol氧气,质量为16g,故D正确;
故答案为C。

【题目】把温度为20 ℃,浓度为1.0 mol/L的H2SO4溶液和2.2 mol/L的碱溶液各50 mL混合[溶液密度均为1g/mL,比热容为4.18 kJ/(kg·℃)]轻轻搅动,测得酸碱混合液的温度变化数据如下:
反应物 | 起始温度t1 ℃ | 终止温度t2 ℃ |
H2SO4+NaOH | 20 | 33.6 |
H2SO4+NH3·H2O | 20 | 32.6 |
(1)反应NH3·H2O(aq)![]() NH4+ (aq)+OH-(aq)的焓变约____。
NH4+ (aq)+OH-(aq)的焓变约____。
(2)计算上述两组实验测出的中和热:ΔH1=___kJ/mol;ΔH2=__kJ/mol。
(3)由本题结论可预测将第1组中的1 mol/L的H2SO4溶液换成2mol/L的CH3COOH溶液进行实验,测得的中和热数值__(填“大于”“小于”或“等于”)56.848。