题目内容
【题目】下列物质(均为中学化学常见物质)转化关系图中,D为红棕色粉末(反应条件及部分反应物、产物未全部说明),B、C、E为常见单质,A、D为氧化物。
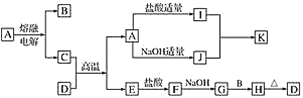
根据图示转化关系填写下列空白:
(1)写出下列物质的化学式A________,B________,G________。
(2)C与D的混合物通常称__________(填名称)。
(3)写出下列化学方程式或离子方程式
①I+J→K________________(离子方程式)。
②G+B→H________________(化学方程式)。
【答案】Al2O3 O2 Fe(OH)2 铝热剂 Al3++3[Al(OH)4]-=4Al(OH)3↓ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
由转化关系图可知,电解A得到B与C,A能与盐酸、氢氧化钠反应,则A为两性氧化物Al2O3、C为Al、B为O2;氯化铝溶液和偏铝酸钠溶液反应生成氢氧化铝和氯化钠,则I为AlCl3、J为Na[Al(OH)4]、K为Al(OH)3;D为红棕色粉末,与Al发生铝热反应得到A与E,则D为Fe2O3, E为Fe,;Fe与盐酸反应生成氯化亚铁和氢气,氯化亚铁与氢氧化钠溶液反应生成氢氧化亚铁,氢氧化亚铁与氧气和水反应生成氢氧化铁,氢氧化铁受热分解生成氧化铁和水,则F为FeCl2、G为Fe(OH)2、H为Fe(OH)3。
(1)由上述分析可知,A为Al2O3,E为Fe,G为Fe(OH)2,故答案为:Al2O3;Fe;Fe(OH)2;
(2)铝和氧化铁的混合物通常称为铝热剂,高温下能发生铝热反应生成氧化铝和铁,故答案为:铝热剂;
(3)①I+J→K的反应为氯化铝溶液和偏铝酸钠溶液反应生成氢氧化铝和氯化钠,反应的离子方程式为Al3++3[Al(OH)4]-=4Al(OH)3↓,故答案为:Al3++3[Al(OH)4]-=4Al(OH)3↓;
②G+B→H的反应为氢氧化亚铁与氧气和水反应生成氢氧化铁,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3。

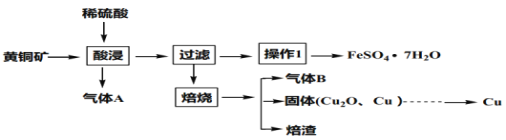
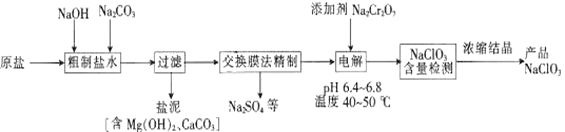
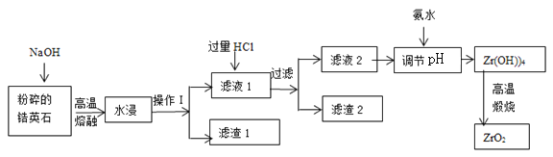
【题目】氧化锆(ZrO2)材料具有高硬度、高熔点、高强度、高韧性、极高的耐磨性及耐化学腐蚀性等优良的物化性能。以锆英石(主要成分为 ZrSiO4,含有少量Al2O3、SiO2、Fe2O3等杂质)为原料通过碱熔法制备氧化锆(ZrO2)的流程如下:
25℃时,有关离子在水溶液中沉淀时的pH数据:
Fe(OH)3 | Zr(OH)4 | Al(OH)3 | |
开始沉淀时pH | 1.9 | 2.2 | 3.4 |
沉淀完全时pH | 3.2 | 3.2 | 4.7 |
请回答下列问题:
(1)流程中旨在提高化学反应速率的措施有________________________________。
(2)操作I的名称是__________________,滤渣1成分为_________,滤渣2的成分为_____________。
(3)锆英石经“高温熔融”转化为Na2ZrO3,写出该反应的化学方程式:____________________。
(4)“调节pH”时,合适的pH范围是__________________。为了得到纯的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是__________________。
(5)写出“高温煅烧”过程的化学方程式________________________________。根据ZrO2的性质,推测其一种用途________________________________。
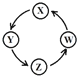
【题目】下列各组物质中,满足表中图示物质在一定条件下一步转化关系的组合有( )
序号 | X | Y | Z | W |
|
① | Si | Na2SiO3 | H2SiO3 | SiO2 | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.②③B.①③④C.①④D.①②③