题目内容
【题目】氢能是一种极具发展潜力的清洁能源。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为___________________________________;该反应自发进行的条件是___________。
(2)Bodensteins研究了如下反应:2HI(g)![]() H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
X(HI) | 1.00 | 0.910 | 0.850 | 0.815 | 0.795 | 0.784 |
X(HI) | 0.00 | 0.600 | 0.730 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:___________。
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=__________min-1(保留三位有效数字)
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。______________

(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________。
【答案】 CH4(g)+O2(g)=CO2(g)+2H2(g) △H3=-689.2KJ·mol-1 任意条件均自发 K=0.1082/0.7842 0.960或19.0  Al-3e-+7 AlCl4—==4 Al2Cl7—
Al-3e-+7 AlCl4—==4 Al2Cl7—
【解析】(1)CH4燃烧的热化学方程式:①CH4(g)+2O2(g)==CO2(g)+2H2O(l), H=-890KJ·mol-1,H2的热值为50.2kJ·g-1,反应热为100.4KJ·mol-1,热化学方程式:②H2(g)+1/2O2(g)== H2O(l), H=-100.4KJ·mol-1;根据盖斯定律:①-②×2,得CH4(g)+O2(g)=CO2(g)+2H2(g) △H3=-689.2KJ·mol-1;该反应为H<0,S>0,任意条件均自发进行反应;正确答案:CH4(g)+O2(g)=CO2(g)+2H2(g) △H3=-689.2KJ·mol-1 ;7任意条件均自发。
(2)(1)2HI(g)![]() H2(g)+I2(g)是反应前后气体物质的量不变的反应;反应后x(HI)=0.784,则x(H2)=x(I2)=0.108,K=
H2(g)+I2(g)是反应前后气体物质的量不变的反应;反应后x(HI)=0.784,则x(H2)=x(I2)=0.108,K=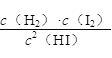 =
= =
=![]() ;正确答案:K=0.1082/0.7842 。
;正确答案:K=0.1082/0.7842 。
(2)到达平衡时,v正=v逆,即k正x2(HI)=k逆x(H2)x(I2),k逆=k正· =k正/K,在t=20 min时,x(H2)= x(I2)=0.045,根据K= k正×k逆,已知k正=9.00min-1,所以k逆= k正/K=9/(0.1082÷0.7842)=473.6,v逆=k逆x(H2)x(I2)= 473.6×(0.045)2=0.96;正确答 案:0.960或19.0。
=k正/K,在t=20 min时,x(H2)= x(I2)=0.045,根据K= k正×k逆,已知k正=9.00min-1,所以k逆= k正/K=9/(0.1082÷0.7842)=473.6,v逆=k逆x(H2)x(I2)= 473.6×(0.045)2=0.96;正确答 案:0.960或19.0。
(3)原平衡时,x(HI)为0.784,x(H2)为0.108,二者图中纵坐标均约为1.6(因为平衡时v正=v逆),升高温度,正、逆反应速率均加快,对应两点在1.6上面,该反应2HI(g)![]() H2(g)+I2(g)△H=+11kJ/mol,升高温度,平衡向正反应方向移动,x(HI)减小,x(H2)增大,据此可以画出图像变化,图像如下:正确答案:
H2(g)+I2(g)△H=+11kJ/mol,升高温度,平衡向正反应方向移动,x(HI)减小,x(H2)增大,据此可以画出图像变化,图像如下:正确答案:

(3)放电时为原电池,金属铝做负极被氧化,根据电子守恒和电荷守恒规律,该极反应为:Al-3e-+7 AlCl4—==4 Al2Cl7—;正确答案:Al-3e-+7 AlCl4—==4 Al2Cl7—。