题目内容
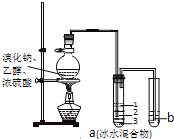
【题目】某固体混合物可能由Al、( NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,现象和有关数据如图所示(气体体积数据换算成标准状况)。关于该固体混合物,下列说法正确的是( )

A.含有4.5gAl
B.不含FeCl2、AlCl3
C.含有物质的量相等的( NH4)2SO4和MgCl2
D.含有MgCl2、FeCl2
【答案】C
【解析】
5.60L标况下的气体通过浓硫酸后,体积变为3.36L,则表明V(H2)=3.36L,V(NH3)=2.24L,从而求出n(H2)=0.15mol,n(NH3)=0.1mol,从而确定混合物中含有Al、( NH4)2SO4;由白色沉淀久置不变色,可得出此沉淀为Mg(OH)2,物质的量为![]() ;由无色溶液中加入少量盐酸,可得白色沉淀,加入过量盐酸,白色沉淀溶解,可确定此沉淀为Al(OH)3,溶液中含有AlCl3。从而确定混合物中一定含有Al、( NH4)2SO4、MgCl2、AlCl3,一定不含有FeCl2。
;由无色溶液中加入少量盐酸,可得白色沉淀,加入过量盐酸,白色沉淀溶解,可确定此沉淀为Al(OH)3,溶液中含有AlCl3。从而确定混合物中一定含有Al、( NH4)2SO4、MgCl2、AlCl3,一定不含有FeCl2。
A. 由前面计算可知,2Al—3H2,n(H2)=0.15mol,n(Al)=0.1mol,质量为2.7g,A错误;
B. 从前面的推断中可确定,混合物中不含FeCl2,但含有AlCl3,B错误;
C. n(NH3)=0.1mol,n[(NH4)2SO4]=0.05mol,n(MgCl2)= n[Mg(OH)2]=0.05mol,从而得出(NH4)2SO4和MgCl2物质的量相等,C正确;
D. 混合物中含有MgCl2,但不含有FeCl2,D错误。
故选C。

【题目】一名同学把4.48 L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8 mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
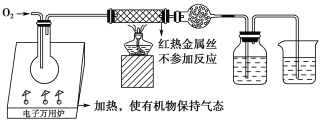
实验结束后发现无水CuSO4变蓝,干燥管和洗气瓶共增重18 g,澄清石灰水变浑浊后又恰好变澄清。请根据实验回答下列问题:
(1)O2要过量的原因是:________________。
(2)若该有机物只含C、H两种元素,且不含任何官能团,也不含脂环,则该有机物的分子式为________,它可能属于________(填序号)。
A.烷烃 B.苯的同系物 C.芳香烃 D.烃的衍生物
该物质可能的结构简式为_____________________。
(3)若该有机物分子中含有一个氧原子,则它可能是哪几类物质?请各举一例,填写在下表中:
物质种类 | 实例(写结构简式) |
_________ | _________ |
_________ | _________ |
_________ | _________ |