题目内容
【题目】香料M的一种合成流程如下:
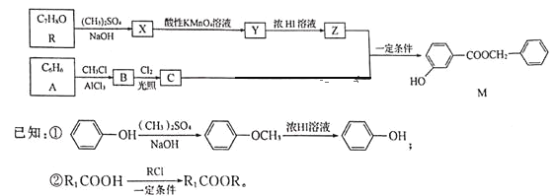
请回答下列问题:
(1)M中含碳的官能团名称是__;设计R→X和Y→Z步骤的目的是__。
(2)A→B的反应类型是___,B的名称是___。
(3)R分子中最多有__个原子共平面。
(4)R和M在下列仪器中信号完全相同的是___(填字母)。
a.质谱仪 b.元素分析仪 c.红外光谱仪 d.核磁共振氢谱仪
(5)写出C和Z反应生成M的化学方程式:___。
(6)在Y的同分异构体中,同时满足下列条件的结构有___种(不考虑立体异构)。
①能发生银镜反应
②遇氯化铁溶液发生显色反应
③1mol有机物最多能消耗3molNaOH
(7)已知苯环上有烃基时,新引入取代基主要取代邻位、对位氢原子。参照上述合成流程,设计以苯和异丙醇为原料制备Br![]() 的合成路线:___(无机试剂任选)
的合成路线:___(无机试剂任选)
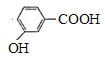
【答案】酯基 保护酚羟基 取代反应 甲苯 14 b ![]() +
+
![]()
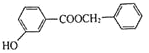 +HCl 10 :CH3CH(OH)CH3
+HCl 10 :CH3CH(OH)CH3![]() CH3CHBrCH3
CH3CHBrCH3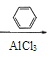
![]()
![]() Br
Br![]()
【解析】
由A的分子式,结合M的结构简式,则A为![]() ,
,![]() 与CH3Cl在无水AlCl3作用下,发生取代反应生成B,则B的结构简式为
与CH3Cl在无水AlCl3作用下,发生取代反应生成B,则B的结构简式为![]() ,B在Cl2在光照条件下反应生成C,C的结构简式为
,B在Cl2在光照条件下反应生成C,C的结构简式为![]() ,Z为
,Z为 ,由R的分子式,结合已知信息①,可知R的结构简式为
,由R的分子式,结合已知信息①,可知R的结构简式为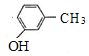 ,X为
,X为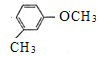 ,X在酸性高锰酸钾溶液作用下被氧化生成Y,Y的结构简式为
,X在酸性高锰酸钾溶液作用下被氧化生成Y,Y的结构简式为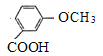 。
。
由分析可知:A为![]() ,B的结构简式为
,B的结构简式为![]() ,,C的结构简式为
,,C的结构简式为![]() ,R的结构简式为
,R的结构简式为 ,X为
,X为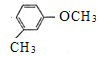 ,Y的结构简式为
,Y的结构简式为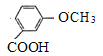 ,Z为
,Z为 。
。
(1)M中含碳的官能团名称是:酯基;设计R→X和Y→Z步骤的目的是保护酚羟基,防止酚羟基被氧化;
(2)A→B是苯环上的H原子被-CH3代替,发生的反应类型是取代反应,B的名称是甲苯;
(3)R的结构简式为 ,旋转单键可以使-CH3中1个H原子、可以使-OH中1个H原子处于苯环的平面上,故最多有14个原子共面;
,旋转单键可以使-CH3中1个H原子、可以使-OH中1个H原子处于苯环的平面上,故最多有14个原子共面;
(4)a.质谱仪是用来测定相对分子质量,R和M的相对分子质量不同,a错误;
b.元素分析仪是用来检测物质中所含的元素,R和M都只含有H、C、O三种元素,所含元素相同,b正确;
c.利用红外光谱可以获得有机物分子中含有何种化学键或官能团信息,R和M含有的官能团与基团不完全相同,c错误;
d.检测有机物分子中不同化学环境中的氢原子,R和M中氢的化学环境不同,d错误;
答案选b;
(5)C和Z反应生成M的化学方程式:![]() +
+
![]()
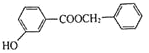 +HCl;
+HCl;
(6)Y(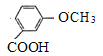 )的同分异构体同时满足下列条件:①能发生银镜反应,说明分子中含有醛基;②遇氯化铁溶液发生显色反应,说明分子中含有酚羟基;③1mol有机物最多能消耗3molNaOH,说明分子中含有酚羟基,-OOCH,还含有-CH3,羟基与甲基在苯环上有邻、间、对3种位置结构,对应的-OOCH,分别有4种、4种、2种结构,故符合条件Y的同分异构体共10种结构;
)的同分异构体同时满足下列条件:①能发生银镜反应,说明分子中含有醛基;②遇氯化铁溶液发生显色反应,说明分子中含有酚羟基;③1mol有机物最多能消耗3molNaOH,说明分子中含有酚羟基,-OOCH,还含有-CH3,羟基与甲基在苯环上有邻、间、对3种位置结构,对应的-OOCH,分别有4种、4种、2种结构,故符合条件Y的同分异构体共10种结构;
(6)由题中信息中定位规律可知:![]() 与溴在催化剂条件下得到目标物。由A→B转化,可知苯与2-溴丙烷得到
与溴在催化剂条件下得到目标物。由A→B转化,可知苯与2-溴丙烷得到![]() 。异丙醇与HBr发生取代反应得到2-溴丙烷。合成路线为:CH3CH(OH)CH3
。异丙醇与HBr发生取代反应得到2-溴丙烷。合成路线为:CH3CH(OH)CH3![]() CH3CHBrCH3
CH3CHBrCH3
![]()
![]() Br
Br![]()

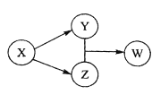
【题目】X、Y、Z、W四种物质的转化关系。下列组合中不符合该关系的是( )
X | Y | Z | W |
| |
A | Na2CO3 | CO2 | CaCO3 | Ca(HCO3)2 | |
B | SO2 | Na2SO3 | H2SO4 | NaHSO3 | |
C | HCl | FeCl2 | Cl2 | FeCl3 | |
D | Na2O2 | NaOH | Na2CO3 | NaHCO3 |
A.AB.BC.CD.D