题目内容
下列离子方程式的书写与所给条件相符的是
| A.将4 molCl2通入到含有4 mol FeBr2的溶液中:2Cl2+2Fe2++2Br-= 4Cl-+Br2+2Fe3+ |
| B.已知亚硫酸(H2SO3)的第二级电离常数K2比偏铝酸(HAlO2)的电离常数K要大,则将少量的SO2气体通入到偏铝酸钠溶液中发生的离子反应是:AlO2-+ SO2+2 H2O =Al(OH)3↓+HSO3- |
| C.稀氨水溶液吸收了少量二氧化碳气体: NH3 ·H2O + CO2 = NH4+ + HCO3- |
| D.在明矾溶液中加入氢氧化钡溶液至沉淀质量达到最大时发生的离子反应是: 2Al3+ +3SO42-+3Ba2++6OH-= 3BaSO4↓+2 Al(OH)3↓ |
A
解析试题分析:A.根据电子守恒,将4 molCl2共得到8mol电子,先和二价铁离子反应,4 mol Fe2+得到4mol电子,还有4molBr-得到电子生成了2molBr2分子,FeBr2的溶液中:2Cl2+2Fe2++2Br-= 4Cl-+Br2+2Fe3+,故正确;B.亚硫酸(H2SO3)的二级电离常数K2比偏铝酸(HAlO2)要大,说明酸性:亚硫酸氢根离子>偏铝酸,则亚硫酸氢根离子也能和偏铝酸钠溶液,所以将少量的SO2气体通入到偏铝酸钠溶液中发生的反应为2AlO2-+SO2+3H2O=2Al(OH)3↓+SO32-,不符合强酸制弱酸的原则,故B错误。C.稀氨水溶液吸收了少量二氧化碳气体应该生成碳酸铵,错误;D.在明矾溶液中加入氢氧化钡溶液至沉淀质量达到最大时只要保证两个物质的量之比是2:3时可达到沉淀量最大,即发生的离子反应是: 3Ba2+ + 3SO42- +2Al3+ + 6OH- ="==2" Al(OH)3↓+3BaSO4
考点:本题考查弱电解质的电离及酸性的比较,利用题给信息进行分析解答是解答本题的关键,难度不大。

正确表示下列化学反应的离子方程式的是( )
| A.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O |
| B.铜片插入硝酸银溶液中 Cu + Ag+ = Cu2+ + Ag |
| C.氢氧化钡溶液与稀硫酸的反应 OH-?+H+= H2O |
| D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.在0.1 mol·L-1 NaOH溶液中:K+、Na+、SO42-、HCO3- |
| B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、Ba2+、NO3-、Cl- |
| C.在0.1 mol·L-1 FeCl3溶液中:K+、NH4+、I-、SCN- |
| D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- |
甲、乙、丙是三种不含相同离子的可溶性电解质。它们所含的离子如下表所示:
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH—、NO3—、SO42— |
取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)>c(乙)>c(丙),下列说法错误的是
A.甲中一定含Na+ B.乙中一定含NH4+
C.丙中一定含Mg2+ D.丙中一定含SO42—
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。
下列说法正确的是
| A.a点对应的溶液中大量存在:Al3+、Na+、Cl-、NO3- |
| B.b点对应的溶液中大量存在:K+、Ba2+、NO3-、I- |
| C.c点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| D.d点对应的溶液中大量存在:Na+、K+、SO32-、Cl- |
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法不正确的是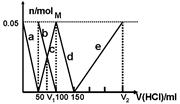
| A.M点时生成的CO2为0mol |
| B.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| C.V1:V2=1:4 |
| D.a曲线表示的离子方程式为:AlO2-+H+ + H2O=Al(OH)3↓ |
能正确表示下列反应的离子方程式是
| A.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-===3Fe3++NO↑+2H2O |
B.三氯化铁浓溶液滴入沸水中,制取氢氧化铁胶体Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
C.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.铝片跟氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑ |
在pH=1的无色溶液中,下列离子能大量共存的是
| A.NH4+、Ba2+、NO3—、CO32— | B.K+、Mg2+、NO3-、SO42— |
| C.Fe2+、OH—、SO42—、MnO4— | D.Na+、Fe3+、Cl—、AlO2— |