题目内容
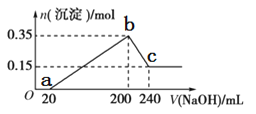
【题目】将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。
(1)写出Al与NaOH溶液反应的化学方程式___________________;
(2)镁和铝的总质量为________g;
(3)b点溶液中的溶质为__________,硫酸的物质的量浓度为___________ mol/L;
(4)生成的氢气在标准状况下的体积为__________L;
(5)c点溶液中通入足量的CO2的反应化学方程式为___________。
【答案】2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 9 Na2SO4 2.5 10.08 NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
【解析】
由图象可知,从开始至加入NaOH溶液20 mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后有剩余,溶液的溶质为H2SO4、MgSO4、Al2(SO4)3,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O;当V(NaOH溶液)=200 mL时,沉淀量最大,此过程中Mg2+、Al3+与OH-反应生成Mg(OH)2和Al(OH)3,溶液溶质为Na2SO4;从200 mL到240 mL,NaOH溶解固体Al(OH)3,发生反应:OH-+ Al(OH)3=AlO2-+2H2O,据此分析解答。
(1)Al与NaOH溶液反应产生NaAlO2和H2,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)根据图象可知Mg(OH)2和Al(OH)3的物质的量之和为0.35 mol,从200 mL到240 mL,NaOH溶解Al(OH)3,当V(NaOH溶液)=240 mL时,沉淀不再减少,此时全部为Mg(OH)2,物质的量为0.15 mol,Al(OH)3的物质的量为0.35 mol-0.15 mol=0.2 mol,由元素守恒可知n(Al)=n[Al(OH)3]=0.20 mol,n(Mg)=n[Mg(OH)2]=0.15 mol,所以镁和铝的总质量为m(Al)+m(Mg)=0.20 mol×27 g/mol+0.15 mol×24 g/mol=9 g;
(3)沉淀量最大时为Mg(OH)2和Al(OH)3,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(Na2SO4)等于200 mLNaOH溶液中含有的n(NaOH)的0.5倍,所以n(Na2SO4)=0.5×5 mol/L×0.2 L =0.5 mol,所以H2SO4的物质的量浓度c(H2SO4)=![]() =2.5 mol/L;
=2.5 mol/L;
(4)根据以上分析,n(Al)=0.2 mol,n(Mg)=0.15 mol,由于Al是+3价金属,Mg是+2价的金属,所以金属失去电子的物质的量n(e-)=3n(Al)+2n(Mg)=0.2 mol×3+ 0.15 mol×2=0.9 mol,根据反应过程中得失电子守恒,可知反应产生氢气的物质的量n(H2)=![]() n(e-)=0.45 mol,则在标准状况下的体积V(H2)=0.45 mol×22.4 L/mol=10.08 L;
n(e-)=0.45 mol,则在标准状况下的体积V(H2)=0.45 mol×22.4 L/mol=10.08 L;
(5)在b点时溶液中溶质为Na2SO4,沉淀量为Mg(OH)2和Al(OH)3,在b→c过程中发生反应:NaOH+Al(OH)3=NaAlO2+2H2O,至c点,该反应恰好反应完全,故c点溶液的溶质为Na2SO4、NaAlO2,由于酸性:H2CO3>Al(OH)3,所以c点溶液中通入足量的CO2,NaAlO2、CO2、H2O反应产生Al(OH)3和NaHCO3,反应的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3。

 阅读快车系列答案
阅读快车系列答案